Door: I.H.M. Friesema, C.M. de Jager, A.E. Heuvelink, W.K. van der Zwaluw, S. Kuiling, J.T.M. Zwartkruis, W. van Pelt
In 2009 werden 38 sporadische patiënten met een Shigatoxineproducerende Escherichia coli (STEC)-O157-infectie gediagnosticeerd (1999-2007: 36-57 per jaar), wat neerkomt op 0,23 ziektegevallen per 100.000 inwoners. Daarnaast was er een landelijke uitbraak met 20 patiënten (1 in 2008 en 19 in 2009). In 2009 werden ook 51 patiënten met een (Shigatoxineproducerende E. coli-stammen)-non-O157-infectie gediagnosticeerd: meest gevonden O-groepen waren O26, O91 en O113. Van de STEC-O157 patiënten in 2009 werd 40% opgenomen in een ziekenhuis (33-54% in eerdere jaren) en ontwikkelde 1 meisje (2%) het hemolytisch-uremisch syndroom (HUS) (8-21% in eerdere jaren). Tien procent van de STEC-non-O157-patiënten werd in het ziekenhuis opgenomen (2008: 14%) en geen van hen ontwikkelde (hemolitisch uremisch syndroom). Consumptie van rauw/ongaar vlees en contact met dieren/mest werd significant vaker gerapporteerd door STEC-non-O157-patiënten ten opzichte van STEC-O157-patiënten en controles. Op basis van de laboratoria die met behulp van (polymerase chain reaction) ook STEC-non-O157 kunnen detecteren, wordt geschat dat het daadwerkelijke aantal STEC-non-O157 In Nederland infecties 3,6 keer hoger is dan het aantal STEC-O157-infecties.
STEC, met als meest bekende serogroep O157, is een bekende verwekker van maagdarmklachten met symptomen variërend van ongecompliceerde diarree tot hemorragische colitis en het HUS. Vooral bij kleine kinderen en ouderen treden complicaties op (1-4). De lage infectieuze dosis van STEC-O157, 1-100 bacteriën, leidt gemakkelijk tot explosies, zoals de uitbraken in Nederland in 2005, 2007 en 2009 (5-7). Herhaaldelijk wordt benadrukt dat ook STEC-non-O157-uitbraken kunnen veroorzaken (8-10) en worden meer zieken met STEC-non-O157 dan met STEC-O157 gevonden (11, 12). Vanwege de ernst van de ziekte bij kleine kinderen en ouderen en het risico op epidemische verspreiding is in Nederland in januari 1999 de geïntensiveerde surveillance van STEC O157 van start gegaan en zijn in december 1999 STEC-infecties opgenomen in de aangifte. In 2007 is de intensieve surveillance uitgebreid met STEC-non-O157, waarbij opgemerkt moet worden dat slechts ongeveer een kwart van de Nederlandse laboratoria technieken gebruikt die het mogelijk maken STEC-non-O157 te detecteren. In dit artikel presenteren we de resultaten van de surveillance voor het jaar 2009.
Methoden
Cases
Elke positieve bevinding van STEC (op basis van fecesonderzoek of serologie) dient door het laboratorium gemeld te worden aan de (Gemeentelijke Gezondheidsdienst). Tot 2007 werd het fecesonderzoek vrijwel altijd gedaan met behulp van een kweek. Echter, de meest gebruikte kweekmethode (afstrijken op sorbitol-MacConkey agar) detecteert alleen sorbitolnegatieve STEC-O157. Sinds 2007 worden door steeds meer Nederlandse laboratoria gebruik gemaakt van een real time polymerase chain reaction methode (rt-PCR) (11, 13) of commerciële kits waarmee alle STEC gedetecteerd kunnen worden.
Alle (Escherichia coli) O157-isolaten worden opgestuurd naar het RIVM. In geval van een positieve rt-PCR of commerciële kituitslag worden na uitplaten van de feces 1 tot 5 willekeurig geselecteerde kolonies opgestuurd. Op het RIVM worden alle ingestuurde E. coli-O157 en mogelijke STEC-non-O157-isolaten met behulp van PCR getest op de aanwezigheid van de belangrijkste virulentiegenen: genen coderend voor Shigatoxinetype 1 en -type 2 (stx1 en stx2), het E. coli attaching and effacing gen ( (E. coli attaching-and-effacing)) en het (Enterohemorragische Escherichia coli)-hemolysinegen (e-hly). Isolaten positief voor (shigatoxine) worden vervolgens getypeerd middels O- en H- serotypering. In geval van STEC-O157 wordt ook bepaald of het isolaat sorbitol-fermenterend is. Tenslotte worden (deoxyribonucleic acid) fingerprints van STEC-O157-isolaten gemaakt door middel van pulsed field gel electroforese (PFGE), waarbij XbaI gebruikt wordt als restrictie-enzym. Isolaten met een minimale overeenkomst van 90% worden beschouwd als ‘mogelijk gerelateerd’ (groep). Isolaten die meer dan 95% overeenkomstige fragmenten hebben, worden benoemd als ‘nauw gerelateerd’ (cluster). Kleinere verschillen binnen 1 cluster worden onderscheiden in subclusters. Clusteranalyse van de fingerprints wordt uitgevoerd met Bionumerics® (Dendrogram type = UPGMA, Similarity coëfficient = Dice).
De GGD verzamelt aan de hand van een standaardvragenlijst voor elke patiënt informatie over het klinische beeld en blootstelling aan bekende risicofactoren. Bij een vermoeden van een bron wordt contact opgenomen met de nVWA te Zutphen voor monstername en onderzoek naar STEC en typering van eventuele isolaten. Door vergelijking van de (pulsed-field gel electroforese)-patronen van isolaten uit voedsel, dieren of omgevingsmonsters met die van de patiënt kan worden bepaald of dit de mogelijke bron van infectie is geweest.
Controles
Sinds juli 2008 wordt elke 3-4 maanden een vergelijkbare vragenlijst naar telkens een nieuwe aselekte steekproef van controlepersonen gestuurd. De adressen zijn afkomstig uit de (bevolkingsregister) van 38 gemeenten verspreid over Nederland. Gegevens uit de vragenlijst van de 3 zendingen van 2009 (maart, juni, oktober) zijn vergeleken met de antwoorden uit de vragenlijsten van de STEC-patiënten. Daarnaast zijn de STEC-patiënten uit 2008 en 2009 samen vergeleken met de 2 zendingen uit 2008 en de 3 zendingen uit 2009.
Resultaten
Meldingen
In 2009 werden 346 patiënten gemeld via de aangifte en/of het insturen van een isolaat. (Tabel 1) Nog eens 9 andere patiënten zijn uit de telling weggelaten. Dit betrof 8 keer een toevalsbevinding, zonder diarreeklachten, die 7 keer niet bevestigd kon worden en 1 keer een STEC-O174:H8-isolaat opleverde. De negende persoon was vorig jaar al met dezelfde STEC-stam (O54:H21) gemeld. Het RIVM ontving 270 isolaten, waarvan bij 108 de aanwezigheid van stx-genen kon worden bevestigd. Voor de overige 162 isolaten kon dit niet door het RIVM worden bevestigd.
In n totaal werden 289 van de 346 patiënten (85%) gemeld via de aangifte, waarbij het laboratorium in 65% van de gevallen binnen 24 uur de positieve bevinding aan de GGD had doorgegeven. Bij 6 patiënten werd gemeld dat ze HUS hadden ontwikkeld. Echter, van 3 patiënten is geen stam ingestuurd en van de overige 3 kon slechts bij 1 een STEC-infectie (STEC-O157-isolaat) bevestigd worden.
De verdere resultaten worden beperkt tot de bevestigde STEC-infecties.
Typering van isolaten
Serotypering van de 108
STEC-isolaten leverde 57 keer serogroep O157 op, waarvan 19
patiënten uit 2009 betrokken waren bij een landelijke uitbraak in
december 2008-januari 2009. (7) De uitbraakstam was een
O157:H-stam, positief voor stx1+2, eae en e-hly. De helft (53,8%)
van de isolaten in 2009 bevatte zowel stx1 als stx2, 43,6% droeg
alleen het stx2-gen en 1 isolaat (2,6%) alleen het stx1-gen.
O157:H7, positief voor alleen stx2 was het meest voorkomend,
gevolgd door O157:H-, stx1+2 en O157:H7, stx1+2 .
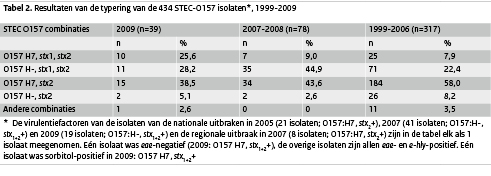
(Tabel 2) Tenslotte was 1 isolaat in 2009 sorbitolfermenterend
(O157:H-, stx1+2).
Van de 51 STEC-non-O157-isolaten was 3 keer de O-groep niet typeerbaar. Bij de overige 48 isolaten werden 26 verschillende O-groepen gevonden. O26 kwam in 2009 het meest voor (tabel 3), gevolgd door O91 en O113. Van de 51 STEC-non-O157-isolaten bevatten 25 isolaten alleen het stx1-gen, 22 isolaten alleen het stx2-gen en 4 isolaten bevatten beide genen. In totaal 13 isolaten hadden het eae- en het e-hly-gen, 12 isolaten hadden alleen het eae-gen, 18 isolaten alleen het e-hly-gen en 8 isolaten geen van beide genen.
Demografische kenmerken en
vragenlijst-gegevens van de patiënten met een
bevestigde STEC-infectie
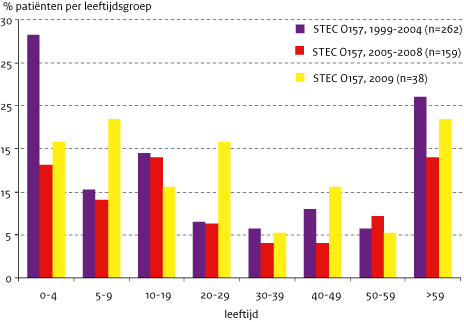
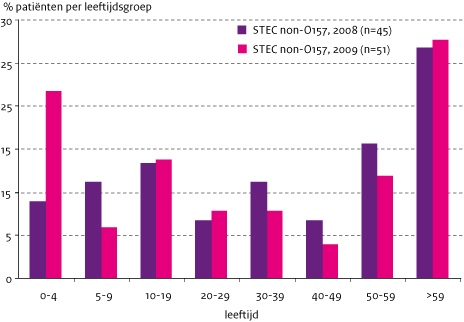
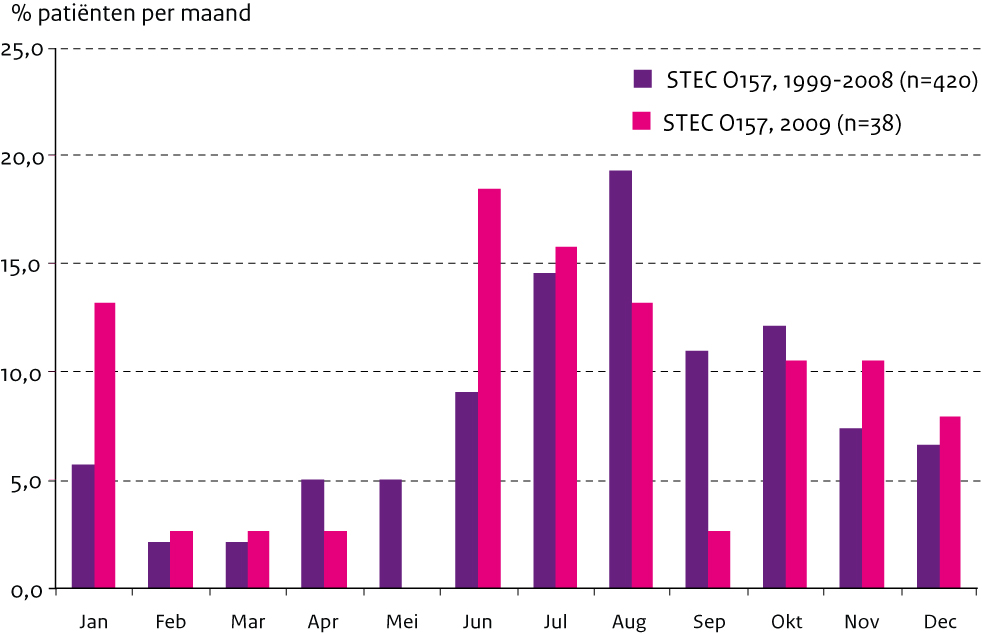
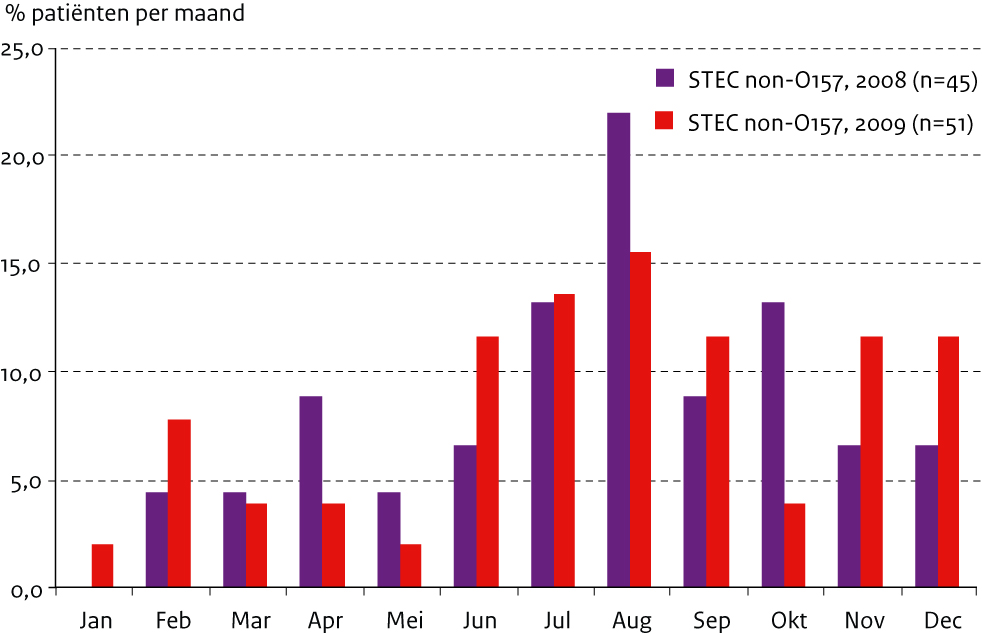
Er werden iets meer vrouwen dan mannen gemeld met een STEC-infectie (58/108, 54%), wat vooral voor de STEC-non-O157-infecties gold (30/51, 59%). Onder de patiënten met een STEC-O157-infectie was de verdeling man:vrouw ongeveer gelijk (29:28). In 2009 waren er relatief veel STEC- O157-patiënten in de leeftijdsgroepen 5-9 en 20-29 jaar ten opzichte van voorgaande jaren, terwijl onder de STEC-non-O157-patiënten vooral veel 0-4 jarigen te zien waren (figuur 1a en 1b). Ook na uitsluiting van de uitbraak in januari 2009 blijft het percentage patiënten met STEC-O157 hoog in januari (figuur 2a). Verder zijn de meeste STEC-O157-patiënten (figuur 2a) in 2009 te zien tussen juni en augustus (47%, 43% over 1999-2008) en voor STEC-non-O157-infecties (figuur 2b) zijn dit de maanden juni tot en met september (53% in 2009 en 51% in 2008). In 2009 werd 40% van de STEC- O157-patiënten opgenomen in het ziekenhuis ten opzichte van 33%-54% in de voorgaande jaren en 10% van de STEC-non-O157-patiënten ten opzichte van 14% in 2008. Eén meisje van 4 jaar ontwikkelde HUS als gevolg van een STEC-O157-infectie (2%; 8-21% voorgaande jaren). Eén vrouw van 91 jaar met een STEC-O17:H41 is overleden, zij was 3 dagen voor het ontstaan van de maagdarm-klachten al in het ziekenhuis opgenomen vanwege algehele achteruitgang van de gezondheid.
Figuur 1a. Percentage patiënten per leeftijdsgroep voor STEC-O157 (1999-2004, 2005-2008 en 2009), exclusief de patiënten van de uitbraken in 2005, 2007 en 2009
Figuur 1b. Percentage patiënten per leeftijdsgroep voor STEC-non-O157 (2008 en 2009)
Figuur 2a. Percentage patiënten per maand voor STEC-O157 (1999-2008 en 2009), exclusief de patiënten van de uitbraken in 2005, 2007 en 2009
Figuur 2b. Percentage patiënten per maand voor STEC-non-O157 (2008 en 2009)
Figuur 3. Percentage STEC-O157-patiënten per risicofactor per jaar (1999-2009), exclusief de STEC-O157-patiënten van de uitbraken in 2005, 2007 en 2009
Doormelden van een positieve bevinding door het laboratorium aan de GGD vond voor 59% van de patiënten plaats binnen de wettelijk vereiste 24 uur (O157 = 29/51; non-O157 = 30/49). In totaal zijn 7 van de bevestigde infecties (5x O157 en 2x non-O157) niet officieel gemeld door de betreffende GGD, voor de 2 patiënten met een STEC-non-O157-infectie is wel een surveillancevragenlijst ingevuld.
Voor 47 (82%) van de STEC-O157-patiënten, waaronder de 19 uitbraakpatiënten, en 26 (51%) van de STEC-non-O157-patiënten in 2009 werd een vragenlijst ingestuurd. De tijd tussen de eerste ziektedag van de patiënt en het invullen van de vragenlijst was voor STEC-O157 mediaan 15 dagen (1-79 dagen) ten opzichte van 13 tot 21 dagen in voorgaande jaren. Voor STEC-non-O157 was de mediaan 30 dagen (10-132 dagen) ten opzichte van 33 dagen in 2008.
De meest gerapporteerde klachten (door meer dan 75%) bij een STEC-O157-infectie zijn diarree (98%), buikpijn en/of buikkramp (98%) en bloed in de ontlasting (85%). Voor STEC-non-O157-infecties waren dit diarree (81%) en buikpijn en/of buikkramp (81%). Op het moment van invullen van de vragenlijst had nog 28% (O157) en 42% (non-O157) van de patiënten klachten. Bij degenen die hersteld waren, had de ziekte mediaan 7 dagen (range 3-38 dagen, O157) geduurd. Bij de patiënten met STEC-non-O157 was dit 9 dagen (2-56 dagen), maar was dit maar bekend voor 7 personen.
Bij de analyse van de risicofactoren zijn de patiënten die betrokken waren bij de landelijke uitbraak van STEC-O157 uitgesloten. De meest waarschijnlijke bron van deze uitbraak was filet américain. Zowel consumptie van rauw vlees als contact met dieren/mest lijkt te stijgen onder patiënten met een STEC-O157-infectie (figuur 3), terwijl consumptie van rauwe melk(producten) en contact met zieken voorafgaand aan eigen ziekte afgenomen zijn. Vergelijking van de risicofactoren tussen STEC-O157, STEC-non-O157 en controlepersonen leverde voor 2009 geen significante verschillen op (tabel 4). Vergelijking van de patiënten uit 2008 en 2009 samen ten opzichte van de controles laat zien dat voor de STEC-non-O157-infecties consumptie van rauw vlees, met name filet américain, en contact met dieren risicofactoren zijn. En dit geldt ten opzichte van zowel de controles als de STEC-O157-infecties.
PFGE-clusteranalyse STEC-O157
Naast de 19 patiënten uit 2009 die gerelateerd waren aan de landelijke uitbraak, was er nog 1 patiënt met een stam die vrijwel identiek is aan die van de uitbraak. Hij was ook in dezelfde periode ziek. Naast de uitbraak waren er in 2009 nog 6 andere clusters, waarvan 4 bestaande uit 2 personen. Eén van deze clusters speelde zich af rond de jaarwisseling met 1 patiënt in 2008 en 1 patiënt in 2009, beiden 1 jaar oud, verder zijn er geen aanwijzingen voor een gezamenlijke bron. Ook bij het tweede cluster zijn de patiënten ongeveer even oud, ditmaal twintigers, maar behalve dat ze in dezelfde regio wonen en er ongeveer een maand tussen beide eerste ziektedagen zat, zijn er geen verdere epidemiologische gegevens beschikbaar. Bij de 2 andere clusters met 2 personen kwam de stam ook al in de voorgaande jaren voor. De eerste ziektedagen lagen 1 tot 2 weken uit elkaar, maar epidemiologische aanwijzingen voor een gemeenschappelijke bron werden niet gevonden. Het vijfde cluster bestaat uit 4 personen, waarvan 2 broertjes. De andere 2 personen werden op dezelfde dag ziek, 4 maanden voor de 2 broertjes. Beiden wonen in dezelfde regio en hadden beiden filet americain gegeten. Het ene broertje had geen filet américain gegeten, van de andere is dat onbekend. Het laatste cluster bestaat uit 5 personen waaronder ditmaal een zoon en moeder uit 1 gezin. De eerste werd eind juni ziek, de andere 4 allemaal eind juli en begin augustus. Het gezin was in Frankrijk geweest, de overige 3 patiënten waren niet in het buitenland geweest. De vragenlijsten leverden geen epidemiologische aanwijzingen voor een gemeenschappelijke bron.
Nader onderzoek naar mogelijke bronnen van infectie
Naar aanleiding van de landelijke uitbraak van STEC-157 in december 2008-januari 2009 heeft de nVWA onderzoek verricht naar de bron. (7) Het voorafgaande epidemiologische onderzoek wees in de richting van rauw rundvlees. Bij een gezin en een individuele patiënt werden restanten van verdachte vleesproducten opgehaald. Daarnaast werden rundergehakt en filet américain van de door de patiënten meest genoemde supermarktketens getest. Het onderzoek door de nVWA leverde geen positieve vleesmonsters meer op. De intensieve trace back leidde tot de meest waarschijnlijke producent van de geconsumeerde filet américain, maar het epidemiologische verband met filet américain kon niet microbiologisch bevestigd worden. Daarnaast heeft de nVWA onderzoek verricht naar filet américain naar aanleiding van een patiënt waarvan de diagnose STEC niet op het RIVM bevestigd kon worden en bij een veehouderij naar aanleiding van een patiënt waarvan geen isolaat ontvangen is. Beide bronopsporingen hebben niet geleid tot de isolatie van STEC-O157.
Discussie
De incidentie van laboratorium bevestigde STEC-O157-infectie was in 2009 vergelijkbaar met voorgaande jaren: 0,23 versus 0,22-0,35 ziektegevallen per 100.000 inwoners (exclusief explosies). Inclusief explosies komt de incidentie van 2009 uit op 0,35 per 100,000 inwoners ten opzichte van 0,33 in 2005 en 0,51 in 2007. Omdat niet alle laboratoria testmethodes gebruiken waarmee alle STEC gedetecteerd kunnen worden, is er alleen landelijke dekking voor STEC-O157. De laboratoria die PCR gebruiken rapporteerden 12 van de 45 O157-infecties (27%) in 2008 en 14 van de 38 sporadische O157-infecties (37%) in 2009. Dit percentage geeft een schatting van de dekking van STEC-non-O157-infecties. De verhouding O157:non-O157 binnen de laboratoria die PCR gebruiken is 1:3,6. Dit is vergelijkbaar met de verhouding van 1:3,5 van het voorgaande jaar en 1:4 gevonden binnen de Nederlandse pilotstudie in 2005/2006 (11). Omgerekend naar heel Nederland zou dit voor 2009 uitkomen op ongeveer 140 STEC-non-O157-cases. De totale incidentie van STEC-infecties zou dan ongeveer 0,86 ziektegevallen per 100.000 inwoners zijn.
Wereldwijd worden O26, O103, O111 en O145, naast O157, het meest in verband gebracht met STEC-infecties (14, 15). In 2009 werden in Duitsland de O-groepen O26, O103 en O91 (16) en in Nederland O26, O91 en O113 het meest gevonden. STEC-O26 wordt in verband gebracht met zowel individuele patiënten als uitbraken (15, 17, 18) en wordt in Duitsland zelfs vaker gerapporteerd dan STEC-O157 (16). STEC-O91 en -O113 worden minder vaak gevonden, maar worden beide in verband gebracht met ziekte bij mensen (15, 18, 19).
De landelijke uitbraak van STEC-O157 in januari 2009 laat opnieuw zien dat consumptie van rauw of halfgaar rundvlees een belangrijke risicofactor voor STEC-infecties is (7). Daarvoor waren er in 2005 een landelijke uitbraak en in 2007 een regionale uitbraak die beide vrijwel zeker ook veroorzaakt waren door filet américain (5, 6). Bij STEC-O157-patiënten is daarnaast sinds de start van de surveillance in 1999 een stijging in de rapportage van consumptie van rauw/ongaar vlees te zien. Echter, vergelijking van consumptie van rauw/ongaar vlees en meer specifiek, filet américain tussen STEC-O157-patiënten en controles liet echter geen significante verschillen zien voor 2008 en 2009. Voor STEC-non-O157-patiënten werd dit verschil wel gevonden, evenals voor contact met dieren. Alhoewel contact met dieren niet uit de risicoanalyse komt voor STEC-O157, is er wel een verband gevonden tussen regionale runderdichtheid en STEC-O157-infecties in de zomer bij kinderen (20).
Sinds de invoering van PCR-technieken door verschillende laboratoria en de uitbreiding van de surveillance met STEC-non-O157 is het aantal onbevestigde monsters sterk gestegen. In 2008 en 2009 konden de ingestuurde isolaten van respectievelijk 63% en 60% van de patiënten niet bevestigd worden. Het aantal bevestigde STEC-O157-infecties is sinds de start van de surveillance in 1999 redelijk constant, waarbij pieken vrijwel geheel door uitbraken veroorzaakt worden. De uitbreiding heeft er toe geleid dat de GGD’en in de gebieden met laboratoria die gebruik maken van PCR beduidend meer meldingen binnenkrijgen. Voor alle gemelde patiënten een surveillancevragenlijst invullen blijkt moeilijk te motiveren zonder bevestiging waardoor GGD’en meestal wachten tot deze binnen is. Hierdoor zit er meer tijd tussen eerste ziektedag en het invullen van de vragenlijst. Daarnaast is ook de druk op het RIVM toegenomen door het gestegen aantal isolaten. Deze situatie is duidelijk niet optimaal en er moet beslist gaan worden welke aanpak de beste combinatie tussen inspanning en opbrengst oplevert. Belangrijk daarbij is dat alle partijen achter de gekozen aanpak staan.
Conclusie
Geconcludeerd wordt dat STEC-non-O157-infecties in Nederland wat betreft incidentie minstens zo belangrijk zijn als STEC-O157-infecties. Wat betreft ziektelast lijken de STEC-non-O157-infecties een minder belangrijke rol te spelen (minder vaak bloederige diarree), wat mede afhankelijk is van welke O-groepen gevonden worden. Meest voorkomende serogroepen in Nederland naast O157 waren in 2009 O26, O91 en O113, die ook wereldwijd regelmatig voorkomen. STEC-O157 blijft in Nederland nog steeds het belangrijkste O-type, wat blijkt uit de aantallen patiënten, de landelijke uitbraak en de overige clusters. We moeten echter niet vergeten dat de surveillance van STEC-non-O157 (nog) niet landelijk dekkend is.
Dankwoord
Wij bedanken alle GGD’en en medisch microbiologische laboratoria hartelijk voor hun medewerking bij de verzameling van de patiëntgegevens en het insturen van isolaten en de medewerkers van de nVWA voor het onderzoek naar landbouwhuisdieren en verdacht voedsel.
|
|
Auteurs
I.H.M. Friesema (1), C.M. de Jager (1), A.E. Heuvelink (2), W.K. van der Zwaluw (1), S. Kuiling (1), J.T.M. Zwartkruis (2), W. van Pelt (1)
1 RIVM, (Centrum Infectieziektebestrijding (onderdeel van het RIVM)), Bilthoven
2 Nieuwe Voedsel en Waren Autoriteit, Regionale Dienst Oost,
Zutphen
Correspondentie:
Literatuur
1. Paton JC, Paton AW. Pathogenesis and diagnosis of Shiga toxin-producing Escherichia coli infections. Clin Microbiol Rev 1998;11(3):450-79.
2. Nataro JP, Kaper JB. Diarrheagenic Escherichia coli. Clin Microbiol Rev 1998;11(1):142-201.
3. Reiss G, Kunz P, Koin D, Keeffe EB. Escherichia coli O157:H7 infection in nursing homes: review of literature and report of recent outbreak. J Am Geriatr Soc 2006;54(4):680-4.
4. Karmali MA. Host and pathogen determinants of verocytotoxin-producing Escherichia coli-associated hemolytic uremic syndrome. Kidney International 2009;75(SUPPL. 112).
5. Doorduyn Y, de Jager CM, van der Zwaluw WK, et al. Shiga toxin-producing Escherichia coli (STEC) O157 outbreak, The Netherlands, September - October 2005. Euro Surveill 2006;11(7):182-5.
6. Friesema I, Sigmundsdottir G, van der Zwaluw K, et al. An international outbreak of shiga toxin-producing Eschericha coli O157 infection due to lettuce, September-October 2007. Euro Surveill 2008;13(50):18-22.
7. Greenland K, de Jager C, Heuvelink A, et al. Nationwide outbreak of STEC O157 infection in the Netherlands, December 2008-January 2009: continuous risk of consuming raw beef products. Euro Surveill 2009;14(8).
8. Schimmer B, Nygard K, Eriksen HM, et al. Outbreak of haemolytic uraemic syndrome in Norway caused by stx2-positive Escherichia coli O103:H25 traced to cured mutton sausages. BMC Infect Dis 2008;8:41.
9. De Schrijver K, Buvens G, Posse B, et al. Outbreak of verocytotoxin-producing E. coli O145 and O26 infections associated with the consumption of ice cream produced at a farm, Belgium, 2007. Euro surveill 2008;13(7).
10. McCall BJ, Slinko VG, Smith HV, et al. An outbreak of shiga toxin-producing Escherichia coli infection associated with a school camp. Commun Dis Intell 2010;34(1):54-6.
11. Van Duynhoven YTHP, Friesema IHM, Schuurman T, et al. Prevalence, characterization and clinical profiles of Shiga toxin-producing Escherichia coli in the Netherlands. Clin Microbiol Infect 2008;14:437-45.
12. Friesema IHM, de Jager CM, Heuvelink (alveolaire echinokokkose), van der Zwaluw WK, Kuiling S, van Pelt W. Intensieve surveillance van Shiga-toxineproducerende Escherichia coli (STEC) in Nederland, 2008. Infectieziekten Bulletin 2010;21(1):12-8.
13. Schuurman T, Roovers A, van der Zwaluw WK, et al. Evaluation of 5’-nuclease and hybridization probe assays for the detection of shiga toxin-producing Escherichia coli in human stools. J Microbiol Methods 2007;70(3):406-15.
14. Perelle S, Dilasser F, Grout J, Fach P. Screening food raw materials for the presence of the world’s most frequent clinical cases of Shiga toxin-encoding Escherichia coli O26, O103, O111, O145 and O157. Int J Food Microbiol 2007;113(3):284-8.
15. Johnson KE, Thorpe CM, Sears CL. The emerging clinical importance of non-O157 shiga toxin-producing Escherichia coli. Clin Infect Dis 2006;43(12):1587-95.
16. Robert-Koch-Institute. SurvStat. 2010. (www3.rki.de/SurvStat). (Accessed 27 juli 2010).
17. Jenkins C, Evans J, Chart H, Willshaw GA, Frankel G. Escherichia coli serogroup O26 - A new look at an old adversary. J Appl Microbiol 2008;104(1):14-25.
18. Bettelheim KA. The non-O157 Shiga-toxigenic (verocytotoxigenic) Escherichia coli; under-rated pathogens. Crit Rev Microbiol 2007;33(1):67-87.
19. Bielaszewska M, Stoewe F, Fruth A, et al. Shiga toxin, cytolethal distending toxin, and hemolysin repertoires in clinical Escherichia coli O91 isolates. J Clin Microbiol 2009;47(7):2061-6.
20. Friesema IH, J VDK, CM DEJ, Heuvelink AE, W VANP. Geographical association between livestock density and human Shiga toxin-producing Escherichia coli O157 infections. Epidemiol Infect 2010:1-7.
Intensive surveillance of Shiga toxin producing Escherichia coli (STEC) in the Netherlands, 2009
In 2009, 38 symptomatic sporadic cases were diagnosed with STEC O157 infection (1999-2007: annually 36 to 57) corresponding with 0.23 sporadic cases per 100,000 inhabitants. A further 20 cases could be related to a national outbreak of whom 19 cases in 2009 and 1 case in 2008. In 2009, 51 cases were diagnosed with a STEC non-O157 infection, with O26, O91 en O113 as most common O-groups. In 2009, 40% of the STEC O157 cases were hospitalized (33-54% in previous years) and 1 girl (2%) developed the haemo-lytic-uraemic syndrome (HUS) (8-21% in previous years). Ten percent of the STEC non-O157 cases were hospitalized (2008: 14%) and none developed HUS. Consumption of raw or undercooked meat and contact with animals was significantly more often reported by STEC non-O157 cases compared to STEC O157 cases and controls. Based upon laboratories using PCR for the detection of STEC, it was estimated that the actual number of STEC non-O157 infections in the Netherlands is about 3.6 times higher than the reported number of STEC O157 infections.