Hier vindt u de artikelen bij de (Antimicrobial Resistance)@RIVM nieuwsbrief voor professionals nummer 8, 2025.
The catch of Type-Ned
CRE25-survey
Het RIVM doet mee aan de “Genomische surveillance van carbapenem-resistente Enterobacterales 2025 (CRE25-survey) in de [ignore]EU/EER” van (European Centre for Disease Prevention and Control)
Carbapenem-resistente Enterobacterales (CRE) vormen een grote bedreiging voor patiënten in zorgsystemen in de landen van de Europese Unie en de Europese Economische Ruimte (EU/EER), zoals beschreven in de derde update van de “rapid risk assessment” van het ECDC [1]. Sinds de survey uit 2019 naar carbapenem- en/of colistine-resistente Enterobacterales (CCRE-survey) zijn er ontwikkelingen die laten zien dat de situatie in de EU/EER verder verslechtert:
- er zijn meer gevallen van bloedbaaninfecties door carbapenem-resistente Klebsiella pneumoniae;
- K. pneumoniae vertoont steeds vaker zowel virulentie (ziekteverwekkend vermogen) als resistentie;
- er worden nieuwe Enterobacterales-soorten met carbapenemase genen ontdekt;
- carbapenemase genen verspreiden zich via plasmiden (overdraagbare genetische elementen);
- er worden steeds meer hoog-risico typen van Escherichia coli gevonden die carbapenemase genen bij zich dragen, met het risico dat deze zich ook buiten ziekenhuizen in de gemeenschap verspreiden [1].
Om een beter beeld te krijgen van de verspreiding van deze hoog-risico typen van K. pneumoniae en E. coli, en om gerichte maatregelen voor infectiepreventie en -bestrijding te kunnen nemen, wordt een nieuwe EU/EER survey gepland voor de periode van 1 oktober t/m 31 december 2025 (CRE25-survey).
Voor deze survey worden Nationale Referentielaboratoria (NRL’s) uit 37 landen die deelnemen aan het European Antimicrobial Resistance Genes Surveillance Network (EURGen-Net) uitgenodigd om whole-genome sequencing (WGS)-gegevens aan te leveren bij het ECDC. Deze gegevens moeten worden aangevuld met gestandaardiseerde epidemiologische en microbiologische metadata, voor maximaal 40 isolaten per NUTS-2-regio, volgens de in dit protocol beschreven criteria.
Het RIVM doet mee met de CRE25-survey. Anders dan bij de eerdere resistentie-gerelateerde surveys zoals de CCRE- en CRAb-surveys, hoeven diagnostische laboratoria of ziekenhuizen geen extra stammen of informatie aan te leveren. Er wordt alleen gebruik gemaakt van typeergegevens die via de lopende Type-Ned-surveillance beschikbaar zijn bij het RIVM. Via de (Antimicrobial Resistance)-nieuwsbrief houden wij u op de hoogte.
Doelstellingen van de CRE25-survey
Het belangrijkste doel van de CRE25-survey op EU/EER-niveau is het vaststellen:
- waar hoog-risico-CRE voorkomen;
- hoe hoog-risico-CRE zich verspreiden; en
- hoe hun populatie zich ontwikkelt.
Hierbij gaat het ook om overdraagbare genetische elementen die van groot belang zijn voor de volksgezondheid binnen zorginstellingen in de EU/EER. Deze informatie helpt bij het verbeteren van risicobeoordelingen en het opstellen van passende maatregelen. Een tweede doel is om deelnemende landen te ondersteunen bij het opbouwen van kennis en vaardigheden voor genomics-gebaseerde surveillance en bij het uitvoeren van risicobeoordelingen van multiresistente ziekteverwekkers met een mogelijk epidemisch karakter.
[1] European Centre for Disease Prevention and Control (ECDC). Carbapenem-resistant Enterobacterales – third update. Stockholm: ECDC; 2025. Available at: https://www.ecdc.europa.eu/en/publications-data/carbapenem-resistant-en…
Cluster van besmettingen met (New Delhi Metallo-β-Lactamase)-5-producerende Enterobacter hormaechei in Nederland en in 5 andere Europese landen
Er wordt onderzoek gedaan naar een genetisch cluster van de Gram-negatieve bacterie Enterobacter hormaechei die ongevoelig is voor carbapenems. Het cluster is aan het licht gekomen in de kiemsurveillance van carbapenemase-producerende Enterobacterales (CPE) die het RIVM uitvoert. De stam van E. hormaechei (behorend tot het Enterobacter cloacae complex) behoort tot multilocus sequence typing (MLST) type ST1344 en bevat het carbapenemase-gen NDM-5. De aanwezigheid van dit gen gaat gepaard met (aangetoonde) fenotypische meropenem-resistentie. De isolaten van dit EclCluster-036-cluster verschillen onderling niet meer dan 4 allelen.
Sinds april 2025 zijn er 14 personen gemeld bij wie bovengenoemde stam is gekweekt: 8 vrouwen en 6 mannen met een mediane leeftijd van 63 jaar (range 40-89 jaar). Bij 7/14 personen werd de bacterie gekweekt uit urine, bij 2/14 uit bloed, en bij 2 andere personen uit drainvocht of punctaatmateriaal van lever/galwegen. Bij de overige 3 personen ging het alleen om een positieve screeningskweek (rectumswab) en betrof het dus kolonisatie. De genoemde kweken zijn afgenomen in april (n=2), mei (n=1), juli (n=5), augustus (n=2) en september (n=4), en zijn ingezonden door 10 verschillende medisch microbiologische laboratoria (MML’s). Het grootste deel van de kweken zijn ziekenhuiskweken die op verschillende afdelingen van 9 verschillende ziekenhuizen zijn afgenomen. Eén kweek werd afgenomen in een huisartsenpraktijk. Slechts 1 persoon was kort voor het afnemen van kweekmateriaal in een buitenlands ziekenhuis opgenomen, en 2 personen waren in het voorgaande jaar in het buitenland geweest zonder dat er sprake was van ziekenhuisopname. De overige patiënten hadden geen bekende reisgeschiedenis. De meeste personen waren wel recent opgenomen in een Nederlands ziekenhuis, en tijdens dergelijke opnames werden ook diverse invasieve ingrepen verricht. Omdat de opnames van de betrokken personen plaatsvonden in verschillende zorginstellingen in het hele land, en er geen epidemiologische links zijn gevonden van betrokken personen met andere personen binnen het cluster, en van betrokken personen met een buitenlands ziekenhuis, is de hypothese dat besmetting plaatsvindt vanuit een gemeenschappelijke puntbron. Hierbij kan gedacht worden aan een medisch hulpmiddel, zorggerelateerde materialen of aan medicatie. Aanvullend onderzoek naar de mogelijke besmettingsbron wordt op dit moment uitgevoerd in samenwerking met betrokken (Gemeentelijke Gezondheidsdienst)’en en (medisch microbiologisch laboratorium)’s.
Na uitvraag door het ECDC bleek dat er in 5 andere Europese landen in de afgelopen maanden bij één of meerdere patiënten eveneens isolaten zijn gevonden die behoren tot EclCluster-036. Ook hier was er meestal geen bekende epidemiologische link met ziekenhuisopname in-, of recent bezoek aan een ander land. Ook ging het in deze landen in het merendeel van de gevallen om patiënten die opgenomen waren in een ziekenhuis. Een en ander versterkt de eerder genoemde hypothese dat er sprake is van een gemeenschappelijke puntbron, die dan dus in meerdere landen voor besmettingen zorgt. Onder aanvoering van het ECDC en het Europese reflab voor AMR (EURL-PH-AMR) wordt ook in deze andere Europese landen verder onderzoek gedaan naar mogelijke bronnen. Uiteraard zullen de bevindingen in Europees verband worden gedeeld, waarna verdere gezamenlijke bron-analyse kan plaatsvinden.
Bronnen: RIVM, ECDC, EURL-PH-AMR.
Seizoensgebonden stijging fusidinezuur-resistente (Methicilline-resistente Staphylococcus aureus) met (Multi-Locus Variable number of tandem repeat Analysis)-type MT4627
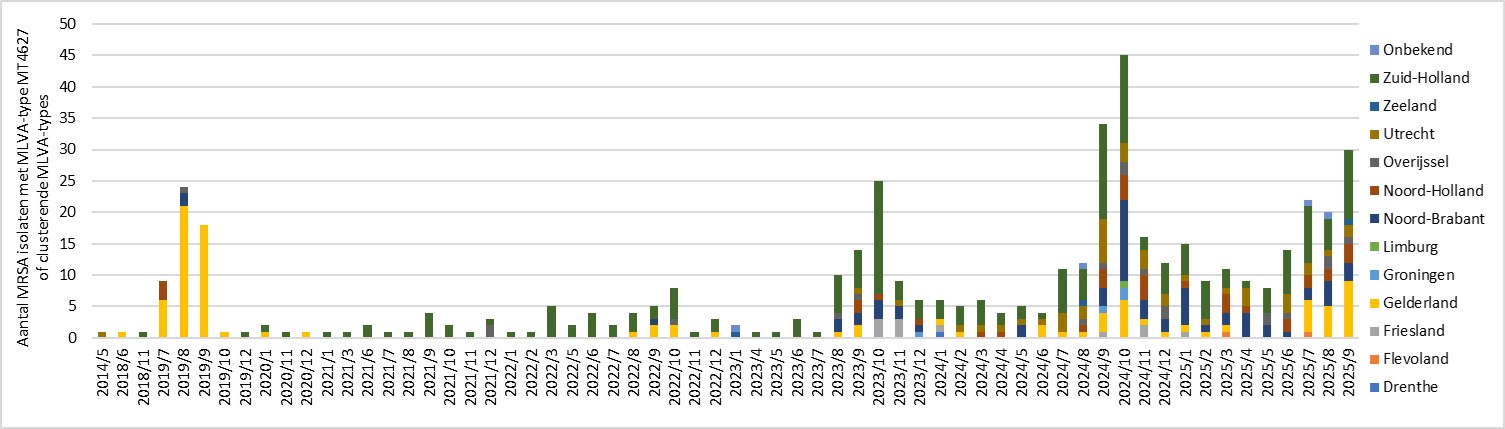
Sinds juni 2025 wordt in de Type-Ned-MRSA-surveillance opnieuw een stijging gezien van het aantal MRSA-isolaten met MLVA-type MT4627 en nauw verwante typen (Figuur 1). Daarnaast komen er vanuit verschillende GGD-regio’s signalen dat er mogelijk lokale clusters van deze typen zijn, conform eerdere jaren. De stijging wordt met name gezien in de provincies Zuid-Holland en Gelderland. MLVA-type MT4627 is geassocieerd met impetigo-uitbraken bij kinderen in de community en piekte de afgelopen jaren ieder jaar tijdens het impetigoseizoen in de nazomer. Dit type is ook in andere landen gevonden met grote mate van verwantschap (Roer L, et al. 2025).
De MRSA-surveillance in het RIVM ontvangt MRSA-isolaten uit heel Nederland, die allemaal middels multiple-locus (Variable-Number Tandem Repeats)-analysis (MLVA) getypeerd worden. Vervolgens wordt een semi-random selectie daarvan gesequenst en nog een deel van de isolaten wordt gesequenst om specifieke redenen (zoals een uitbraak). MLVA-type MT4627 blijkt op basis van whole-genome multilocus sequence typing (wgMLST) genetisch vaak nauw verwant te zijn aan een aantal andere MLVA-types: MT7224, MT7913, MT7837, MT7467 en MT7437. Dus ook wanneer deze andere types worden gevonden, kan er sprake zijn van directe transmissie.
In 2025 tot en met september zijn 138 isolaten met deze 6 MLVA-types ingestuurd naar Type-Ned MRSA, waarvan 59% (81/138) afkomstig was uit infectie-gerelateerd kweekmateriaal. Van deze isolaten was 54% (44/81) afkomstig van kinderen van 0 tot 9 jaar. Hoe vaak de diagnose impetigo is gesteld bij bovengenoemde MLVA-types is niet uit de surveillance data af te leiden. Aangezien er ook veel isolaten uit dragerschapskweken en van volwassenen zijn ingestuurd, betreft het niet uitsluitend patiënten met impetigo. Door de aanwezigheid van exfoliatieve toxine genen is deze stam ook in staat staphylococcal scalded skin syndrome te veroorzaken, wat een enkele keer bij pasgeborenen is gezien afgelopen jaren. Deze informatie wordt niet systematisch verzameld.
In totaal zijn 19 van de 138 (14%) MRSA-isolaten met deze 6 MLVA-types uit 2025 aanvullend getypeerd met (whole genome multi-locus sequence-typing). Bij analyse van alleen de 2025-data zijn hiermee vier genetische clusters (cut-off allelverschil ≤15) gevonden met een grootte van 2 tot 7 personen per cluster. Voor zover bekend waren de personen binnen deze clusters geen huisgenoten en was er dus sprake van verspreiding anders dan uitsluitend binnen gezinnen. De clusters verschillen onderling slechts 26 tot 38 allelen en bij analyse van alle jaren samen behoren alle gesequenste isolaten grotendeels wel tot één cluster. Dit wijst op doorgaande transmissie van deze MRSA in de afgelopen jaren.
Extramurale clusters met MRSA-infecties zijn meldingsplichtig bij de GGD, maar zijn voor medisch microbiologische laboratoria vaak lastig te herkennen. Bovendien wordt er bij impetigo vaak niet gekweekt, waardoor er sprake is van onderrapportage. Soms worden clusters alleen opgepikt door de Type-Ned MRSA-surveillance. Hierdoor komen clusters niet volledig of vertraagd in beeld met als gevolg dat er geen adequate interventies kunnen worden ingezet om verdere verspreiding van MRSA te beperken. Anderzijds is het niet uitgesloten dat de toename in MRSA-detecties met deze MLVA-typen mede wordt veroorzaakt door toegenomen alertheid onder huisartsen, waardoor er sneller wordt gekweekt bij impetigo die niet adequaat reageert op de ingestelde antibiotische behandeling (NHG-bericht december 2024).
Figuur 1. Aantallen MRSA-isolaten met MLVA-type MT4627 of genetisch nauw verwante MLVA-types* per maand, gekleurd op provincie (situatie op 10-10-2025, september mogelijk nog niet compleet)
* Dit betreft de volgende MLVA-types: MT4627 (n=468), MT7224 (n=12), MT7437 (n=1), MT7467 (n=1), MT7837 (n=1) en MT7913 (n=1).
MT4627 bevat het fusidinezuur-resistentiegen fusC. Er zijn ook andere MLVA-types met dit fusC gen. Er wordt al een aantal jaar een stijging gezien in het percentage MRSA-infectie-isolaten met de top 10 meest voorkomende MLVA-types die dit fusC gen bevatten (van 10% (145/1478) in 2019 naar 17% (384/2322) in 2024).
De schatten van ISIS-AR
(Doctor of Philosophy)-student Sophie van Kessel werkt aan haar promotieonderzoek met de titel ‘i3-AMR: van informatie naar inzicht naar interventie voor de bestrijding van antibioticaresistentie’. Een van haar onderzoeksprojecten ging over het effect van watervrij werken op intensive care units op de detectie van gram-negatieve bacteriën bij patiënten met behulp van data in (Infectious Disease Surveillance Information System for Antibiotic Resistance). Zïj schreef de resultaten in een manuscript:
- Water-free care in Dutch (intensive care unit) patient rooms: impact on gram-negative bacteria detections – S.A.M. van Kessel, A.F. Schoffelen, K.H.S. van Son, D.W. Notermans, J.A. Severin, F. Bakhshi-Raiez, F. Velthuis, M. Schipper, D. Dongelmans, A. Verbon, C.C.H. Wielders, on behalf of the ISIS-AR study group
PhD-student Manon Brekelmans heeft een project uitgevoerd waarin ze heeft geëvalueerd of nationale geautomatiseerde surveillance van hospital-onset bacteriemieën kan worden uitgevoerd door data uit ISIS-AR te gebruiken. De resultaten zijn verwerkt in een manuscript:
- Evaluation of national automated surveillance of Hospital Onset Bacteraemia and Fungemia based on the Dutch Infectious Diseases Surveillance Information System – Antimicrobial Resistance (ISIS-AR) – M. Brekelmans, T. van der Kooi, A.F. Schoffelen, R. Zoetigheid, M.S.M. van Mourik, S.C. de Greeff, S. van Rooden, ISIS-AR study group
Recente publicaties met data uit ISIS-AR
- The use of a Poisson bidden Markov model for automated detection of hospital outbreaks with vancomycin-resistant enterococci in routine surveillance data – S.A.M. van Kessel, et al, on behalf of the ISIS-AR study group, on behalf of the (Signaleringsoverleg Zorginstellingen / Antimicrobiële Resistentie) study group, J Hosp Infect 2025
- Clinical prevalence of collateral sensitivity: a systematic exploration of multi-center antimicrobial surveillance data – S.T. Tandar, et al, on behalf of the ISIS-AR study group, accepted for publication in The Lancet Microbe.
Eenheid van Taal en ISIS-AR
Op dit moment leveren 35 (medisch microbiologisch laboratorium)’s data aan ISIS-AR via Eenheid van Taal.
Hepatitis C pilot surveillance
Het RIVM heeft in samenwerking met het Amsterdam (Universitair Medisch Centrum) een pilot moleculaire surveillance voor Hepatitis C-virus (HCV) opgestart. Het doel van de pilot is om inzicht te krijgen in de meerwaarde van whole genome sequencing (WGS) bij het identificeren of bevestigen van transmissienetwerken van (hepatitis C virus) onder (mannen die seks hebben met mannen) in Nederland ter ondersteuning van bron- en contactonderzoek (BCO).
Het aantal acute HCV-infecties is op dit moment stabiel laag met ongeveer 30 cases per jaar. Eerdere genoomsurveillanceanalyses (MS-TRACE) door het AUMC lieten zien dat nieuwe HCV-infecties regelmatig een bron in het buitenland hebben. Anderzijds laten infecties met een Nederlandse bron zien dat, ondanks de effectieve behandeling, er nog steeds transmissie plaatsvindt, met name binnen de populatie van MSM. Dit kan mogelijk verklaard worden door late behandeling of omdat de infectie bij de index nog niet is gediagnosticeerd. Met de komst van zeer effectieve direct acting antivirals (DAA) voor de behandeling van hepatitis C is eliminatie van deze infectie, die wereldwijd elk jaar zo’n 300.000 mensen het leven kost, theoretisch mogelijk geworden. In 2016 heeft de WHO een resolutie aangenomen met als doel eliminatie van virale hepatitis voor 2030 (WHO 2016). Ook Nederland heeft zich, met het Nationaal hepatitisplan en een geplande update hiervan, gecommitteerd aan dit eliminatiedoel.
In deze eliminatiefase is moleculaire surveillance een belangrijk hulpmiddel om transmissienetwerken beter te begrijpen en kan het beleidsbeslissingen ondersteunen bij eventuele (lokale) verheffingen. Met de nieuwe behandeling van hepatitis C bestaat theoretisch de kans op de verspreiding van resistente stammen. Bij de pilot zal daarom ook worden gekeken naar het voorkomen van DAA-geassocieerde resistentiemutaties onder MSM in Nederland, om eventuele introducties en/of verspreiding van resistente stammen vroegtijdig te identificeren.