Redactioneel
Het toenemende gebruik van nanomaterialen vraagt om
duidelijkheid: wat valt wel en niet onder ‘nano’? De Europese
Commissie pakte de handschoen op. Zij kwam in 2011 met een
‘aanbeveling’ voor de algemene contouren voor een nanodefinitie. De
Commissie liet bewust de nadere invulling over bijvoorbeeld
veiligheidseisen, risicobeoordeling en communicatie aan de
specifieke beleidskaders over. De open einden die er in de
Commissieaanbeveling zijn, werken door bij de verfijning in deze
kaders. 'Nano' laat zich nog moeilijk in hokjes plaatsen,
terwijl onze huidige wet- en regelgeving daar wel om vraagt. Een
grote uitdaging, want een definitie is een belangrijke eerste stap
voor passende risicobeheersing en -communicatie voor
nanomaterialen. Denk bijvoorbeeld aan de nano-etiketten op
consumentenproducten.
Het ingeslagen pad in EU (Europese Unie) is vol voetangels en klemmen, en de
praktijk gaat leren of het systeem sluitend is. Het goede is dat
het proces in een open dialoog plaatsvindt, belanghebbenden spreken
zich uit en de onzekerheden liggen op tafel.
ARBO (Arbeidsomstandigheden)
Nanocentre.nl – website voor MKB (Midden- en kleinbedrijf)-bedrijven met vragen over nano
MKB-bedrijven gaven eerder aan behoefte te hebben aan handzame informatie rond veilig werken met nanotechnologie. De website Nanocentre.nl moet deze ondersteuning bieden. Lees meer
Verantwoord gebruik van nanomaterialen in onderzoekslaboratoria
Talloze onderzoeksinstellingen maken of gebruiken nanomaterialen. De veiligheid van werknemers krijgt daarbij vanzelfsprekend aandacht. Aanvullende ondersteuning is nodig om veilig werken nog beter te garanderen. Lees meer
Geneesmiddelen en Medische Technologie
Bijeenkomst Nationaal Platform Nanomedicine
KIR-nano organiseerde in november 2012 een geslaagde bijeenkomst van het Nationaal Platform Nanomedicine. Betrokkenen uit het veld discussieerden over kansen en risico’s van nano-toepassingen in de medische wereld, en of bestaande regelgeving en richtsnoeren volstaan om veiligheid en werkzaamheid te waarborgen. Lees meer
Consument en Voeding
SCCS (scientific committee on consumer safety)-Opinie over gebruik van nanozinkoxide in zonnebrandcrèmes
Het EU Scientific Committee on Consumer Safety (SCCS) velde onlangs een oordeel over volksgezondheidsrisico’s van zonnebrandcrèmes met nanozinkoxide. De wetenschappers geven groen licht voor crèmes, voor sprays ligt het anders. Lees meer
Risicobeoordeling van nanomaterialen in cosmetica in Europa
Hoe gaat Europa om met de risicoschatting van nanomaterialen in cosmetica? Gaat het opgezette ‘check and balances’ systeem de consument voldoende beschermen? Lees meer
Inademen van nanodeeltjes uit cosmetische poederproducten
Verschillende consumentenproducten bevatten tegenwoordig nanodeeltjes. Bij het gebruik van cosmetische poederproducten ligt blootstelling aan zulke deeltjes via de huid voor de hand, en niet via inademing. De praktijk laat anders zien. Lees meer
Ontwikkelingen database consumentenproducten met nanomaterialen
Een up-to-date overzicht van welke consumentenproducten welke nanomaterialen bevatten, lijkt ideaal. Verschillende EU lidstaten zetten daarvoor databases op. Nederland houdt een open blik voor de beste oplossing. Lees meer
Milieu
Milieueffecten van zinkoxide-nanodeeltjes: kennis en kennislacunes
Nanodeeltjes van zinkoxide zitten onder meer als UV (ultraviolet)-filter in zonnebrandcrèmes. Een deel daarvan zal vrijkomen in het milieu. De kennis over de invloed op het leven in water en bodem breidt zich uit. Lees meer
Oplosbaarheid van nanomaterialen en gevolgen voor toxiciteit
Onderzoekers krijgen steeds meer grip op wat de toxiciteit van metaalachtige nanodeeltjes bepaalt. Wetmatigheden uit de milieuchemie en –toxicologie voor de ‘gewone’ metalen komen ook hier naar voren. Lees meer
Verwijdering nanodeeltjes in huisvuilverbrandingsinstallaties
Nanomaterialen in producten belanden uiteindelijk via het afval in huisvuilverbrandingsinstallaties. Sommige deeltjes worden daar volledig verwijderd. Andere nanodeeltjes ontstaan juist in de afvalverwerking, en komen vrij in de lucht. Lees meer
Overige
Europese Commissie publiceert ‘Second Regulatory Review on Nanomaterials’
De Europese Commissie probeert langs diverse wegen vorm te geven aan wet- en regelgeving voor nanomaterialen. Brussel laveert in een mijnenveld. Lees meer
Europese consumentenorganisatie wil aanpassing nanodefinitie in Cosmeticaverordening
De nieuwe Europese wetgeving rond cosmetica richt zich nadrukkelijk op nanomaterialen in consumentenproducten. In onvoldoende mate, stelt de Europese consumentenorganisatie. Een nauwere definitie van wat wel en niet ‘nano’ is zou de consument beter beschermen. Lees meer
Beleidsontwikkelingen in Verenigde Staten
Europa worstelt met het maken van passende wet- en regelgeving voor veilig gebruik van nanomaterialen. Ook de VS (Verenigde Staten) hebben nog geen passend antwoord. Lees meer
Vertering van nanomaterialen en ontstaan ziektes
De kennis over het lot van nanomaterialen in het menselijk lichaam neemt toe. Wat gebeurt er met nanomaterialen wanneer ze in cellen terechtkomen? Spelen ze ook een rol bij het ontstaan van bepaalde ziektes? Lees meer
Naast deeltjes en vezels, nu ook ’nanostrookjes’
De markt heeft ‘nanostrookjes’ ontdekt voor toepassing in bijvoorbeeld zonnepanelen. Het gaat niet alleen om een andere vorm dan deeltjes en vezels, maar ook om andere effecten. Lees meer
ARBO
Nanocentre.nl – website voor MKB-bedrijven met vragen over nano
In 2011 onderzochten Nanohouse, RIVM en TNO, in opdracht van het
Ministerie van Sociale Zaken en Werkgelegenheid (SZW) en het
Ministerie van Economische Zaken (EZ), de informatiebehoefte van
bedrijven rond nanotechnologie. Hieruit kwam naar voren dat
bedrijven behoefte hebben bij het vinden van relevante
veiligheidsinformatie. Belangrijk is dat men ergens terecht kan met
vragen. Bedrijven willen, bijvoorbeeld, weten hoe gevaarlijk
nanodeeltjes zijn, wanneer je eraan wordt blootgesteld, en wat je
aan maatregelen moet nemen om veilig te kunnen werken.
Op 2 oktober 2012 is de website Nanocentre online gegaan.
Nanocentre richt zich in het bijzonder op MKB-bedrijven in
Nederland. Dit platform biedt bedrijven relevante en actuele
informatie die nodig is om veilig met nanomaterialen te kunnen
werken. Op de website kunnen bedrijven vragen stellen over
veiligheid van nanomaterialen, of zelf antwoorden vinden. Ook
kunnen bedrijven via Nanocentre deelnemen aan netwerkbijeenkomsten
over kansen en risico’s van nanomaterialen. Nanocentre is
geïnitieerd door TNO in samenwerking met Syntens Innovatiecentrum
en RIVM. Syntens beantwoordt vragen over mogelijke toepassingen,
terwijl RIVM ondersteuning biedt bij het beantwoorden van vragen
over risico’s van nanomaterialen. RIVM signaleert tevens
onderwerpen voor de nieuwsbrief van Nanocentre.
class="underline">RIVM/KIR-overweging: Nanocentre is
een belangrijk platform waar het MKB terecht kan voor vragen en
ondersteuning over veilig werken met nanomaterialen. De verwachting
is dat deze website voorziet in de eerder gesignaleerde behoefte en
een belangrijke bijdrage levert aan het veilig omgaan met
nanomaterialen op de werkplek. Signalen uit de praktijk zijn ook
belangrijk voor het verder vormgeven van het beleid rond
nanotechnologie.
Verantwoord gebruik van nanomaterialen in onderzoekslaboratoria
Bijna iedere universiteit in Nederland
werkt tegenwoordig met nanomaterialen, onder meer in chemie,
natuurkunde, voeding en geneeskunde. Wetenschappers ontwikkelen
veelal ook nieuwe nanomaterialen. Slechts een beperkt aantal
onderzoeksgroepen heeft eigen beleid ontwikkeld voor het veilig
werken met nanomaterialen. Daarnaast hebben externe partijen
diverse algemene handreikingen en modellen gemaakt voor een
risico-inschatting op de werkplek.
De praktijk laat zien dat onderzoekinstellingen onvoldoende uit de
voeten kunnen met de bestaande hulpmiddelen. Hier zijn diverse
oorzaken voor: de hulpmiddelen passen niet bij de situatie, ze zijn
te aspecifiek om een betrouwbare uitspraak te kunnen doen, en ze
geven verschillende uitkomsten in vergelijkbare situaties.
De Stichting voor Fundamenteel Onderzoek der Materie (FOM) heeft
met TNO, het FOM-instituut voor Atoom en Molecuulfysica (AMOLF),
Technische Universiteit Delft en Universiteit Leiden een project
opgezet rond veilig werken met nanomaterialen in een
onderzoeksomgeving. Het plan is om te analyseren welke hulpmiddelen
er worden gebruikt en hoe groot het aantal mogelijk blootgestelde
werknemers in de sector is. Daarnaast komt er een handleiding over
welke in de literatuur beschreven modellen geschikt zijn binnen een
onderzoeksomgeving en welke randvoorwaarden daarbij van belang
zijn. Tot slot besteedt het project ook aandacht aan risicobeheer
en -communicatie. Dit is in de vorm van een praktische handleiding
voor het omgaan met nanomaterialen en de daarbij behorende onzekere
risico’s.
RIVM/KIR-overweging: Er zijn veel verschillende handleidingen en
hulpmiddelen beschikbaar voor het veilig werken met synthetische
nanomaterialen. Het RIVM onderschrijft het belang van het
ontwikkelen van richtlijnen voor veilig werken met nanomaterialen
in onderzoeksomgevingen.
Geneesmiddelen en Medische Technologie
Bijeenkomst Nationaal Platform Nanomedicine
De tweede bijeenkomst van het
Nationaal Platform Nanomedicine 1 heeft plaatsgevonden
op 15 november 2012. Deze bijeenkomst was in samenwerking met
NanoNextNL/thema NanoMedicine georganiseerd. Tijdens de
bijeenkomsten hebben ongeveer 40 belanghebbenden gediscussieerd
over technische en beleidsrelevante ontwikkelingen rond
nanomedicine. Het gaat hierbij om zowel kansen als risico’s van
nanomedicine in brede zin: de focus ligt op alle toepassingen van
nanotechnologieën bij geneesmiddelen, medische hulpmiddelen en
combinatieproducten.
De deelnemers zijn geïnformeerd over de nanomedicine-activiteiten
binnen het nationale onderzoeksprogramma NanoNext.NL. Daarnaast stonden twee
inhoudelijke thema’s op de agenda: “Kwaliteit, veiligheid &
werkzaamheid van ‘nanosimilars’ ” en ‘Top 3 van ziekten uit de RIVM
VolksgezondheidsToekomstVerkenning (VTV): welke kansen biedt
nanomedicine?’
De discussie over nanosimilars lichten we hieronder toe als
voorbeeld van het nut van een multi-stakeholder platform.
Met de term ‘nanosimilar’ wordt bedoeld: kopieën van
nanogeneesmiddelen. Van geneesmiddelen worden na verloop van
patentrechten vaak goedkopere kopieën ontwikkeld. Deze noemen we
‘generieken’ in geval van geneesmiddelen met een laag
molecuulgewicht (bijvoorbeeld paracetamol), en ‘biosimilars’ voor
biologische geneesmiddelen zoals therapeutische eiwitten
(bijvoorbeeld groeihormoon). Voor het op de markt brengen van een
generiek geneesmiddel volstaat een combinatie van bewijs dat de
actieve stof identiek is en dat het geneesmiddel een vergelijkbare
biobeschikbaarheid heeft. Voor biosimilars zijn de datavereisten
strenger, omdat het complexe moleculen zijn, waarvan het onmogelijk
is om aan te tonen dat ze identiek zijn.
Recente publicaties van onder andere Schellekens en
collega’s.(2011) en Borchard en
collega’s.(2012) laten zien dat ook voor complexe,
niet-biologische geneesmiddelen zoals liposomen en nano-ijzer
preparaten de klassieke markttoelatingsmethode voor generieken niet
voldoet. Borchard en collega’s geven hierbij voor nano-ijzer
voorbeelden van patiënten met ernstige bloedarmoede die anders
reageerden op de ‘kopieën’ dan op het originele product. De
European Medicines Agency (EMA) onderkent de problematiek
(EMA,
2011a;
EMA, 2011b).
De deelnemers van de platformbijeenkomst onderschreven het belang
voor de patiënt van een relatief snelle ‘generieke’ of ‘similar’
route om producten toe te laten tot de markt. De crux zit in de
noodzaak en diepgang van aanvullende vragen ter beoordeling van de
kwaliteit, veiligheid en werkzaamheid van kopieën. Naarmate er meer
ervaring met een bepaald type ‘similar’ geneesmiddel is opgedaan,
komt scherper vast te staan welke aspecten cruciaal zijn om de
vergelijkbaarheid vast te stellen.
De vergelijkbaarheid van nanomaterialen is een onderwerp dat ook in
verschillende andere beoordelingskaders speelt (alle nanomaterialen
individueel beoordelen, of kun je groeperen?). Kennis uit de
medische hoek draagt nadrukkelijk bij aan kennisontwikkeling in die
andere kaders, en omgekeerd.
RIVM/KIR-overweging: De discussie over nanosimilars laat opnieuw
het belang zien van dialoog tussen verschillende ketenpartners. Het
Nationaal Platform NanoMedicine biedt het forum voor een dergelijke
dialoog. Op relatief informele wijze delen de verschillende
stakeholders hun gezichtspunten, waardoor wetenschap én beleid
vooruitgang kunnen boeken. De KIR-nano- paraplu zorgt bovendien
voor kennisuitwisseling tussen de beleidskaders, bijvoorbeeld
biociden, medicijnen en cosmetica.
1 In opdracht van de Interdepartementale Werkgroep Risico’s Nanotechnologie georganiseerd door KIR-Nano.
Consument en Voeding
SCCS-Opinie over gebruik van nano-zinkoxide in zonnebrandcrèmes
Op 18 september 2012 heeft SCCS
een Opinie aangenomen over zinkoxide (ZnO; in nanovorm) voor
gebruik als UV-filter in zonnebrandcrèmes. De Opinie is
gepubliceerd voor een commentaarronde die liep tot 22 oktober jl.
Recentelijk heeft de EU een voor consumenten toegankelijke
samenvatting van de Opinie op hun website geplaatst. De Opinie
gaat in op de beoordeling van een aantal specifiek gecoate en
ongecoate zinkoxide-nanomaterialen. De algemene conclusie is dat
het gebruik van crème met deze nanodeeltjes net zo veilig is als de
conventionele zonnebrandmiddelen. De beschikbare informatie geeft
aan dat het onwaarschijnlijk is dat zinkoxide-nanodeeltjes via de
huid in het lichaam komen. Bovendien is de hoeveelheid zinkionen
die vrij kunnen komen vanuit de nanodeeltjes en vervolgens het
lichaam binnendringen via de huid, waarschijnlijk onbeduidend laag.
Natuurlijk kunnen zinkionen worden opgenomen wanneer per ongeluk
zinkoxide-nanodeeltjes worden ingeslikt. Het is echter aannemelijk
dat blootstelling via deze route maar marginaal zal plaatsvinden.
Via beide opnameroutes, dus huid en mond, treden er naar
verwachting geen gezondheidseffecten op voor de
zinkoxide-nanodeeltjes.
De SCCS beschouwt echter de toepassing van zinkoxide in
“spray”-producten als niet veilig. Na inhalatie van de
zinkoxide-nanodeeltjes zijn er duidelijk schadelijke effecten
waarneembaar in de long. Volgens de informatie van de
cosmetica-industrie, zijn er op dit moment geen zonnebrandmiddelen
met zinkoxide-nanodeeltjes als spray product op de markt.
De bovengenoemde ‘populaire’ samenvatting geeft een goede
beschrijving van de Opinie over zinkoxide-nanodeeltjes in
zonnebrandcrèmes. Een belangrijke beperking uit de Opinie ontbreekt
echter in deze samenvatting, namelijk dat de conclusies alleen
geldend voor zinkoxide- nanodeeltjes met dezelfde eigenschappen als
die zijn beoordeeld door de SCCS. Tenslotte bevat de Opinie de
‘disclaimer’ dat er in de toekomst extra gegevens nodig zouden
kunnen zijn door een toename in kennis over risico’s van
nanotechnologie. Op die manier kan een (her)beoordeling
plaatsvinden op basis van voortschrijdend inzicht en nieuwe
gegevens.
RIVM/KIR-overweging: Zinkoxide kan via radicaalvorming tot
DNA (deoxyribonucleic acid)-beschadiging kan leiden en dit kan vervolgens een eerste stap
tot tumorvoming zijn. Bij de toepassing van zinkoxide in
zonnebrandcrèmes zijn er nadrukkelijk geen aanwijzingen gevonden
dat dit gebeurt. Het gebruik van zinkoxide als UV-filter geeft
juist een bescherming tegen het ontstaan van huidtum_oren als
gevolg van UV-straling. De Opinie geeft een duidelijke boodschap
af, namelijk dat het gebruik van zinkoxide nanomateriaal veilig is
in zonnebrandcrèmes. De Opinie beschouwt bovendien een groep van
zinkoxide-nanomaterialen van verschillende producenten. Dit wijkt
af van de heersende aanpak om elk nanomateriaal afzonderlijk te
onderzoeken op veiligheid. SCCS stelt dat er voor de onderzochte
zinkoxide-nanomaterialen voldoende overeenkomsten zijn om deze als
groep te beoordelen. Ook zinkoxide-nanomaterialen van andere
producenten vallen onder de beoordeling. Voorwaarde is dat deze
vergelijkbaar zijn wat betreft grootte, zuiverheid, “coating” en
oplosbaarheid. De Opinie geeft hiervoor duidelijke marges.
Risicobeoordeling van nanomaterialen in cosmetica in Europa
De risicobeoordeling van
nanomaterialen in consumentenproducten, zoals cosmetica, is
complex. Dit komt onder meer door de grote variatie in
eigenschappen van nanomaterialen waardoor het risico per toepassing
moet worden bekeken. Henkler en collega’s.
(2012) zetten de verschillende stappen rond de risicoschatting
op een rij. Zij namen hierbij de nieuwe Cosmeticaverordening die
juli 2013 van kracht wordt, als uitgangspunt.
Het algemene richtsnoer voor de veiligheidsbeoordeling van
ingrediënten van cosmetica is de
“Notes of Guidance for the Testing of Cosmetic Ingredients and
their Safety Evaluation”. Deze verwijst onder meer naar de
OESO (Organisatie voor Economische Samenwerking en Ontwikkeling)-richtlijnen voor het testen van chemicaliën. Speciale
notificatieprocedures gelden voor conserveermiddelen, kleurstoffen
en UV-filters, waarbij een veiligheidstoestemming nodig is van de
Scientific Committee on Consumer Safety (SCCS) voordat het
ingrediënt op de markt komt. In het richtsnoer zijn ook algemene
aspecten opgenomen voor het testen van nanomaterialen als
ingrediënt voor cosmetica.
In de nieuwe verordening zal een rechtspersoon 6 maanden voor
plaatsing van een product met een nano-ingrediënt op de Europese
markt, dit moeten melden aan de Europese Commissie (EC).
Specificaties die vereist zijn bij een dergelijke kennisgeving zijn
deeltjesgrootte, gebruikte grondstoffen en informatie over
onzuiverheden in het product. Het toxicologische profiel van het
nano-ingrediënt moet helder zijn voor alle relevante eindpunten met
bijzondere aandacht voor de lokale huidreactie, zoals huid- en
oogirritatie, huidsensibilisatie, en bij UV-filters voor de
fototoxiciteit. Daarna kan de commissie besluiten om de SCCS een
opinie te laten opstellen (binnen 6 maanden) wanneer er zorgen zijn
over de veiligheid. Dit proces kan ook nog plaatsvinden nadat een
product op de markt is gekomen, bijvoorbeeld wanneer er sprake is
van nieuwe wetenschappelijke informatie of nieuwe data over
blootstelling of toxiciteit van het specifieke nanomateriaal. De
SCCS heeft voor de beoordeling van de nanomaterialen als
cosmetica-ingrediënt een speciaal richtsnoer ontwikkeld:
“Guidance on the safety assessment of nanomaterials in
cosmetics”. Deze gaat in op belangrijke aspecten voor de
risicobeoordeling, zoals een goede karakterisering van het
nanomateriaal en het bepalen van de meest relevante
blootstellingsroute(s). Inmiddels heeft de SCCS twee nanomaterialen
beoordeeld die worden gebruikt als UV-filter (ETH-50 en ZnO,
zie elders in deze signaleringsbrief).
Daarnaast is de EC (European Commission) verantwoordelijk voor maatregelen voor markt- en
veiligheidstoezicht en zal een up-to-date ‘catalogus’ van
nanomaterialen in cosmetica worden opgesteld. Een dergelijke
catalogus geeft een overzicht van de gebruikte nanomaterialen in de
cosmetische producten, inclusief gedetailleerde gegevens van de
materialen. Deze catalogus zal gedeeltelijk openbaar zijn voor het
publiek, de bedrijfsgevoelige details zijn niet openbaar.
RIVM/KIR-overweging: De Cosmeticaverordening vormt een van de
eerste wettelijke kaders waar de etikettering en markttoelating van
nanomaterialen is geregeld. De ervaring zal leren of de door
industrie aan te leveren informatie over blootstelling via de huid
en deeltjesgrootte voldoende is, of dat verdere toetsing door de
SCCS nodig is. Er zijn echter al aanwijzingen dat blootstelling via
de huid alleen mogelijk tekort schiet (zie
elders in deze signaleringsbrief). Een grote uitdaging zal
voorlopig zijn hoe om te gaan met (net) afwijkende eigenschappen
(deeltjesgrootte, coating, etc). De “Guidance on the safety
assessment of nanomaterials in cosmetics” zal fabrikanten helpen om
een keuze te maken voor de testen die zij kunnen doen om de
veiligheid van nanomaterialen in cosmetica aan te tonen.
Inademen van nanodeeltjes uit cosmetische poederproducten
Amerikaanse onderzoekers hebben onlangs onderzocht in
hoeverre het mogelijk is om nanodeeltjes te inhaleren die in
cosmetische poederproducten zitten. Uit de studie blijkt dat er
opname van nanostructuren plaatsvindt, voornamelijk van
agglomeraten die groter zijn dan de 1-100 nanometer (nm)
aerosolfractie. Dit heeft tot gevolg dat de deeltjes voornamelijk
terechtkomen in de hogere luchtwegen, en niet in de diepe
luchtwegen, zoals verwacht op basis van de oorspronkelijke
nanodeeltjes.
Nazarenko en
collega’s.(2012) onderzochten drie verschillende cosmetische
poederproducten met een ‘nanoclaim’: de fabrikant geeft aan dat ze
nanomaterialen bevatten. Het gaat om een vochtinbrengend poeder,
een rouge en een los, poedervormig zonnebrandproduct, allen
afkomstig uit de Woodrow Wilson database. Daarnaast zijn drie
controlepoeders onderzocht met een vergelijkbare toepassing, maar
zonder nanoclaim.
In eerste instantie werden de poeders geanalyseerd in hun originele
staat, zoals in de verpakking, met behulp van
transmissie-elektronenmicroscopie (TEM) en
laser-diffractiespectrometrie (LDS). Daarnaast bootsten de
onderzoekers het gebruik van de poeders en de resulterende
inhalatieblootstelling na in een experimentele opstelling door een
hoofd van een etalagepop in een gesloten ruimte te plaatsen.
Als eerste bleek de nanoclaim niet voor alle poeders te kloppen:
een poeder dat gebaseerd zou zijn op nanotechnologie bleek geen
nanodeeltjes te bevatten. De hoogste concentratie nanodeeltjes was
juist terug te vinden in een controlepoeder, dus zonder claim. De
gevonden deeltjes na aanbrengen van het product waren voornamelijk
tussen de 25 nm en 20 micrometer (μm) groot. De hoeveelheid
deeltjes (in aantallen) tussen 100 nm en 20μm varieerde enorm
tussen de verschillende poeders. Alle poeders lieten deeltjes in
deze range zien, zonder grote verschillen tussen de nano- en
controlepoeders. Het is bijzonder dat alle poeders grote deeltjes
(20μm en groter) genereren. De nanodeeltjes moeten daarvoor in de
cosmetische nanopoeders samenklonteren tot agglomeraten van 100 nm
tot 20μm.
Nanodeeltjes kunnen dus aanwezig zijn in alle fracties in de
ademwolk en afzetting van deze nanodeeltjes kan daarom plaatsvinden
in alle delen van het ademhalingssysteem. Omdat de meeste deeltjes
relatief groot zijn, komen de nanostructuren voornamelijk in de
hogere luchtwegen terecht. Dit betekent dat er wellicht andere
gezondheidseffecten te verwachten zijn dan die gebaseerd op de
huidige kennis van het gedrag en effecten van nanodeeltjes diep in
de longen.
RIVM/KIR overweging: Dit is de eerste studie naar de kans op humane
blootstelling aan via inademen van nanomaterialen vanuit
poederproducten voor consumenten. Niet eerder lag de focus op
consumentenblootstelling aan een poederproduct in een dergelijk
realistisch blootstellingscenario. Dit was wel eerder gedaan voor
sprayproducten. Nu blijkt dat nanodeeltjes in poedervorm vooral
grote agglomeraten vormen die in andere delen van de long terecht
kunnen komen dan primaire nanodeeltjes, of agglomeraten kleiner dan
100 nm. Dit heeft gevolgen voor de eventuele gezondheidseffecten in
de long na blootstelling aan nanodeeltjes. De consument kan
hierdoor een aanzienlijk deel van de nanodeeltjes ophoesten of
inslikken. Orale blootstelling lijkt daarom ook een relatief
belangrijke blootstellingsroute.
Het is belangrijk om voor consumentenproducten met nanomaterialen
niet alleen metingen in het product te doen, maar ook een
realistisch blootstellingscenario te testen. Daarbij moet de
aandacht bij de blootstelling na inademen niet alleen uitgaan naar
sprays, maar ook naar cosmetische poederproducten.
De fabrikant is verplicht om ‘nano’ op het etiket te zetten, indien
aan de orde (etikettering; zie elders in deze signaleringsbrief).
De in dit onderzoek aangetroffen situatie van ‘geen nanoclaim, maar
wel nanodeeltjes’ mag niet voorkomen.
Ontwikkelingen database consumentenproducten met nanomaterialen
In 2009 kaartte het Europese Parlement (EP) in een
resolutie het gebrek aan duidelijke informatie aan over het
daadwerkelijk gebruik van nanomaterialen in consumentenproducten.
Het EP verzocht vervolgens de Europese Commissie (EC) om binnen
twee jaar alle relevante wetgeving te (her)beoordelen om daarmee de
veiligheid te waarborgen van alle toepassingen van nanomaterialen
in producten voor mens en milieu gedurende de gehele levenscyclus.
Bovendien is de EC gevraagd om vóór juni 2011 een publiek
toegankelijke inventarisatie te maken van de verschillende soorten
nanomaterialen en het gebruik ervan op de Europese markt. Tot nu
toe is deze inventarisatie op Europees niveau nog niet van de grond
gekomen. Alleen Frankrijk heeft inmiddels een wettelijke regeling
getroffen om een eigen database te bouwen van producten met
nanomaterialen. In een aantal andere Europese lidstaten zijn
inmiddels ook ontwikkelingen gaande rond registratie van
consumentenproducten met nanomaterialen.
Deze ontwikkelingen zijn samengevat in de volgende tabel (met
dank aan P. van Broekhuizen, IVAM (Research and Consultancy on Sustainability of the University of Amsterdam), project Tracing Nano for
Downstream Users and Consumers):
MNM: manufactured nanomaterial
|
|
Frankrijk |
België |
Denemarken |
Italië |
|---|---|---|---|---|
|
Registratie |
verplicht |
verplicht |
Verplicht |
vrijwillig |
|
Te registreren |
nanodeeltjes mengsels artikelen waaruit deeltjes vrijkomen |
class="aligncenter">nanodeeltjes mengsels artikelen waaruit deeltjes vrijkomen |
class="aligncenter">produkten waaruit nanodeeltjes vrijkomen |
nanodeeltjes mengsels artikelen |
|
Traceerbaarheid |
ja, naam van stof en produkt |
ja |
nee, alleen importeurs en producenten |
ja |
|
Wanneer van kracht |
2013 |
2013 |
2013 |
2013 |
|
Verwachte eerst meldingen |
2013 |
2014 |
2014 |
? |
De meest recente ontwikkeling is de Deense aankondiging om ook
een nationale database op te zetten. Op die manier wil de Deense
overheid de kennis en controle over de nanomaterialen op hun markt
vergroten. Bovendien hebben zij de intentie om in een later stadium
deze database als basis voor een eventuele Europese database te
laten dienen (zie persbericht
in het Deens).
Er zijn nog geen aanwijzingen dat Nederland voornemens is om ook
een nationale database op te zetten. Wel brengt KIR-nano, in
opdracht van de VWS (Ministerie van Volksgezondheid, Welzijn en Sport) (en in afstemming met de Interdepartementale
Werkgroep Risico’s Nanotechnologie), momenteel de meningen in kaart
van de verschillende stakeholders (beleid, toezichthoudende
instanties, industrie en ngo’s) over een eventuele Europese
database. Hiervoor is op 30 oktober jl. een discussiepanel
georganiseerd. Glbaal kan gezegd worden dat naar voren kwam dat
draagvlak verkregen kan worden als de noodzaak en doelen van zo’n
database scherp zijn. Daarna komt haalbaarheid en inhoud aan de
orde. Als hoofddoelen van een mogelijke database/registratie kwamen
transparantie naar de consument en traceerbaarheid in de keten voor
ARBO, volksgezondheid en milieuveiligheid naar voren. Ook werden
andere mogelijkheden dan een database genoemd om dit doel te
bereiken. De rapportage zal begin 2013 gereed zijn.
RIVM/KIR overweging: In steeds meer
EU-lidstaten tekent zich de behoefte af om goed in kaart te brengen
welke producten met nanomaterialen op de (consumenten)markt
aanwezig zijn. Enerzijds willen overheden een indruk krijgen in
welke producten nanomaterialen daadwerkelijk worden verwerkt, maar
ze willen ook inschatten of deze nanomaterialen een risico vormen
voor mens en milieu. Punt is dat productie-identificatie versus
risicoschatting een verschillende opzet van een database vragen
(zie “Development
of an inventory for consumer products containing
nanomaterials”). De vraag is ook of er enige kans van slagen is
om de diverse nationale initiatieven op termijn samen te voegen in
een Europese database. Voor een open Europese markt lijkt een
Europese aanpak echter essentieel. Het is daarom nu al van groot
belang om de informatievereisten zorgvuldig te kiezen. Nederland
houdt vooralsnog ook andere opties dan een database open. KIR-nano
volgt de internationale ontwikkelingen rondom databases
nauwlettend.
Milieu
Milieueffecten van zinkoxide-nanodeeltjes: kennis en kennislacunes
Amerikaanse onderzoekers Ma en
collega's (2013) hebben recent een overzichtsartikel
gepubliceerd over de effecten van de nanovorm van zinkoxide op
water- en bodemorganismen. Het artikel is gebaseerd op een
uitgebreide literatuurstudie. Naast het weergeven van de
verschillende effectniveaus uit de diverse studies, gaan de auteurs
tevens in op het onderliggende werkingsmechanisme. De vorming van
zinkionen verklaart voor een groot deel de waargenomen
milieueffecten van zinkoxide-nanodeeltjes. Ook identificeren de
onderzoekers de belangrijkste kennislacunes.
Een van de belangrijkste bevindingen van het artikel is dat het
moeilijk is om alle effectgegevens die over nanodeeltjes van
zinkoxide zijn gerapporteerd, onder één noemer te brengen. Het gaat
steeds om deeltjes van verschillende grootte. Het gedrag van die
deeltjes is op verschillende manieren bepaald, waardoor de
blootstelling van de organismen in de verschillende testen niet te
vergelijken is. Ook constateren de auteurs een tekort aan
langetermijnstudies en wijzen zij op mogelijke stapeling van
niet-opgeloste nanodeeltjes in de voedselketen.
RIVM/KIR-overweging: De studie geeft
een mooi overzicht van de beschikbare toxiciteitsgegevens van
zinkoxide in nanovorm in het milieu. Ondanks de genoemde
verschillen in grootte en gedrag lijkt de hoeveelheid en kwaliteit
van de gegevens zo hoog dat de resultaten van het overzichtsartikel
direct bruikbaar zijn voor een eventuele risicobeoordeling van de
nanovorm van zinkoxide. Een gebrek aan toxiciteitsgegevens na
langetermijnblootstelling is deels pragmatisch te ondervangen door
uit te gaan van de hypothese dat in langetermijnstudies de
zinkoxidedeeltjes oplossen en vrije (toxische) zinkionen vormen.
Van zinkionen is voldoende kennis aanwezig over chronische toxische
effecten.
Oplosbaarheid van nanomaterialen en gevolgen voor toxiciteit
Bij het testen van de toxiciteit van metaalachtige
nanodeeltjes 2 is het belangrijk om rekening te
houden met de (snelheid van de) oplosbaarheid van deze deeltjes.
Hierbij komen ionen in oplossing die toxisch kunnen zijn voor mens
en milieu. De opgeloste nanodeeltjes van zilver leiden bijvoorbeeld
tot relatief hoge gehaltes van toxische zilverionen. Dit geldt ook
voor andere metalen zoals koper en zink
(zie ook elders in deze signaleringsbrief). Om de opname en
toxiciteit van deze nanodeeltjes goed te kunnen bepalen is de
oplosbaarheid cruciaal. De snelheid van oplossen hangt onder meer
af van de samenstelling van het testmedium. Het is dan ook van
belang om bij de bepaling van de toxiciteit van nanodeeltjes
nadrukkelijk rekening te houden met de oploskinetiek van de
gebruikte nanodeeltjes en met de toxiciteit van de gevormde ionen
in het testmedium.
Misra en
collega's (2012) gaven recent een overzicht van de
momenteel beschikbare kennis over het oplossen van nanodeeltjes.
Daarnaast doen zij aanbevelingen om de oplosbaarheid van
nanodeeltjes expliciet te meten in media voor toxiciteitstesten met
nanodeeltjes.
RIVM/KIR-overweging: De Misra studie
geeft een nuttig overzicht van aandachtspunten bij de
risicobeoordeling van metaalachtige nanodeeltjes. Net als bij
reguliere metalen spelen oploskinetiek en biologische
beschikbaarheid een belangrijke rol. Bij het bepalen van de
effecten is aandacht nodig voor het feit dat de toxiciteit van de
deeltjes de som is van de toxiciteit van de niet opgeloste fractie
nanodeeltjes én van de gevormde metaalionen. Daar waar de kennis
over de risicobeoordeling van de metaalionen inmiddels een sterke
basis heeft, zijn er rond de risicobeoordeling van nanodeeltjes nog
diverse kennislacunes.
2 Metaalachtige nanodeeltjes zijn nanodeeltjes die voor een groot deel bestaan uit metalen en /of metaaloxiden.
Verwijdering nanodeeltjes in huisvuilverbrandingsinstallaties
Van sommige nanodeeltjes is bekend dat ze bestand zijn tegen
hoge temperaturen. Recent onderzoek (Wiesner en Plata,
2012) toont aan dat dit ook geldt voor nanodeeltjes van
ceriumoxide (grootte 80 nanometer) en dat ze daarmee ook in tact
blijven tijdens de verbrandingsprocessen in een standaard
afvalverwerkingsbedrijf. Ook vonden de wetenschappers dat de
deeltjes in de afvalgassen terecht kwamen. Ze bleken echter
vervolgens volledig door de roetfilters uit de afvalgassen te
worden weggevangen. Naast dit ‘goede nieuws’ liet het onderzoek ook
zien dat andere metalen, zoals ijzer, aluminium, en silicium, uit
het afval kunnen vervluchtigen en ná passage van de filters en
afkoelen van de afvalgassen, alsnog nieuwe nanodeeltjes kunnen
vormen. Die ‘spontane’ deeltjes komen dan ongestoord vrij in het
milieu vanuit de verbrandingsinstallatie. Het gaat hierbij
overigens niet alleen om metaalachtige nanodeeltjes, maar ook om
koolstofnanodeeltjes zoals fullereenachtige verbindingen (holle
koolstofbollen of –buisjes). De auteurs pleiten voor nader
onderzoek naar mogelijke effecten van deze nieuwgevormde
nanodeeltjes op onze leefomgeving.
RIVM/KIR-overweging: De studie
bevestigt dat nanodeeltjes vrijkomen uit verbrandingsinstallaties.
Dit kunnen zelfs nanodeeltjes zijn die niet in de oorspronkelijke
afvalstroom zaten. Voor een deel is dit niets nieuws onder de zon,
omdat al langer bekend is dat bij verbrandingsprocessen zeer kleine
deeltjes vrijkomen ongeacht de brandstof. De vraag is in welke mate
de samenstelling is veranderd sinds de introductie van synthetische
nanomaterialen. Daar is nog weinig over bekend.
Overige
Europese Commissie publiceert ‘Second Regulatory Review on Nanomaterials’
Na een eerste communicatie over “Regulatory
Aspects of Nanomaterials” in 2008 heeft de Europese Commissie
(EC) een “Second
Regulatory Review on Nanomaterials” gepubliceerd waarin
aandacht uitgaat naar het verbeteren van de EU-wetgeving om een
veilig gebruik van nanomaterialen beter te kunnen garanderen. Het
document wordt vergezeld van een
“Commision Staff Working Paper” dat meer in detail ingaat op
verschillende typen nanomaterialen en verschillende toepassingen,
inclusief veiligheidsaspecten.
De Commissie benadrukt dat mogelijke risico’s van nanomaterialen
afhankelijk zijn van het specifieke materiaal en de specifieke
toepassing. Zij pleit daarom voor een ‘case-by-case’- benadering
(per nanomateriaal en per toepassing) van de risicobeoordeling.
Hierbij zijn de huidige risicobeoordelingsmethoden bruikbaar,
ondanks dat aanpassing van specifieke aspecten van
risicobeoordeling nog nodig is.
De voorgestelde definitie zal waar nodig opgenomen worden in
Europese wetgeving en momenteel wordt gewerkt aan (validatie van)
methoden voor detectie, meten en monitoren van nanomaterialen voor
een juiste inbedding van de definitie. Samen met (ontwikkeling van)
de juiste instrumenten en het vaststellen van gevaren en
blootstellingen zijn dit momenteel de grote uitdagingen op gebied
van reguleren van nanomaterialen.
De EC blijft van mening dat REACH (Registration, Evaluation, Authorisation and restriction of Chemicals) het beste beleidskader is voor
risicobeheersing van nanomaterialen als ze vóórkomen als stoffen of
mengsels. Een aantal aanpassingen van REACH is daarvoor wel nodig.
De EC is voornemens om een aantal van de REACH-bijlagen te wijzigen
en moedigt ECHA (European Chemicals Agency) aan om de richtsnoeren voor registratie verder te
ontwikkelen op het gebied van nanomaterialen na 2013.
Reacties op deze publicatie bleven niet lang uit. Al een dag later
reageerden o.a. (onder andere) het
European Trade Union Institute (ETUI) en het Center for
International Environmental Law op hun websites.
Een grote groep van belangenverenigingen 1 heeft de
commentaren gebundeld in een
brief aan de Commissie. In niet mis te verstane bewoordingen
stellen zij dat de review inconsistent is met de onderliggende
Staff Working Paper en de conclusies van deze paper lijken op hun
beurt inconsistent met de gerapporteerde studies. Verder
concludeert de groep dat met haar weigering om een
voorzorgbenadering te implementeren en de industriebelangen boven
het welzijn van de maatschappij te plaatsen, de Commissie het
verzamelen van uitgebreide data over gevaren en risico’s van
nanomaterialen alleen maar vertraagt en daarmee ook de ontwikkeling
en toepassing van risicobeheersende maatregelen.
RIVM/KIR-overweging: De “Second
Regulatory Review on Nanomaterials” geeft een goed overzicht van de
vorderingen die sinds 2008 zijn gemaakt. Het laat echter ook zien
dat de vorderingen beperkt zijn. Het verschijnen van de
Aanbeveling van de definitie is uiteraard een grote stap, maar
implementatie hiervan in wetgeving is nog beperkt. Vooralsnog is
deze alleen ingevoegd in biocidenwetgeving
(Verordening (EU) No 528/2012) en etikettering van
voedingsmiddelen.
(Verordening
(EU) No 1169/2011), en momenteel lopen discussies over
aanpassing van de definitie in de cosmeticawetgeving (zie
elders in deze signaleringsbrief).
De kritiek op het gebrek aan bescherming van werknemers lijkt
(deels) terecht. In de Staff Working Paper geeft de Commissie aan
dat momenteel niet altijd duidelijk is of een product een
nanomateriaal is of nanomaterialen bevat. Hierdoor is het lastig om
te beslissen of en zo ja welke beschermende maatregelen
noodzakelijk zijn. Voor het verkrijgen van duidelijkheid over
aanwezigheid van nanomaterialen en/of blootstelling daaraan, is
aanpassing van wetgeving essentieel. Pas in 2014 wordt echter een
beoordeling van betreffende wetgeving verwacht, dus pas dan zullen
discussies over mogelijke aanpassing echt starten.
Het beleidskader van REACH is in principe wel geschikt, omdat het
gegevens over de blootstelling en gevaren van chemische stoffen op
kan leveren. Wel zijn aanpassingen nodig om dit voldoende geschikt
te maken voor nanomaterialen. Voorbereidingen op REACH-aanpassingen
zijn weliswaar al in 2008 gestart met het instellen van de CASG
Nano 2, maar desondanks zijn de vorderingen tot nu toe
beperkt. Los van aanpassingen van richtsnoeren, zoals recent
doorgevoerd, is een aanpassing van de REACH-verordening zelf (of
een aanvulling op REACH) essentieel. Belangrijke punten voor de
Nederlandse overheid zijn: de definitie van een nanomateriaal
ontbreekt in REACH, de tonnagegrenzen voor de
informatieverplichtingen zijn te hoog voor nanomaterialen, de
termijn waarbinnen bedrijven de informatie moeten aanleveren is te
lang en, tenslotte ontbreken specifieke vereisten voor de
karakterisering en testen van nanomaterialen in REACH (zie
ook Signaleringsbrief KIR-nano 2012 nummer 2; en de brief
van de Minister van Buitenlandse Zaken aan de Tweede Kamer over
de publicatie van de Commissie).
Het voorstel van de Commissie om alleen de Bijlagen aan te passen
is te verdedigen, omdat de besluitvormingsprocedure daarvoor
eenvoudiger en sneller kan verlopen dan aanpassing van de
hoofdtekst, hetgeen een volledige herziening van de
REACH-verordening vereist. Het opnemen van de definitie en de
tonnagegrenzen lijkt echter meer op zijn plaats in de hoofdtekst.
Omdat de Bijlagen ook wettelijk bindend zijn, zou de mogelijkheid
om aanpassing van REACH voor nanomaterialen volledig in de Bijlagen
onder te brengen, onderzocht kunnen worden.
Voor een goede harmonisatie en implementatie van regelgeving voor
nanomaterialen is aanpassing van alleen de REACH-verordening niet
voldoende. Ook in andere regelgeving, zoals die voor specifieke
productgroepen (gewasbeschermingsmiddelen, biociden, cosmetica,
etiketteringsverordening, etc.), veiligheid en gezondheid op de
werkvloer, of het milieu (geïntegreerde preventie en bestrijding
van verontreiniging (IPPC), Kaderrichtlijn Water, afvalwetgeving),
is naar verwachting (verdere) aanpassing nodig.
1 European
Environment Bureau, European Trade Union Institute,
European Consu
Organisation -BEUC, European Environmental Citizens’
Organisation for Standardisation - ECOS, European Consumer Voice in Standardisation -
ANEC, Women in
Europe for a Common Future, Centre for International Environmental
Law, ClientEarth, Friends of the Earth Germany - BUND
e.V. , en Friends of the Earth Europe
2 Competent Authorities for REACH and CLP (Classification, Labelling and Packaging)
(CARACAL) Subgroup on Nanomaterials.
Europese consumentenorganisatie wil aanpassing nanodefinitie in Cosmeticaverordening
De herziening van de cosmeticaregelgeving van eind 2009
(Verordening (EC) 1223/2009) omvat het gebruik van
nanomaterialen in cosmetica. Hierin is ook een definitie van
nanomaterialen opgenomen. Deze stemt echter niet (meer) overeen met
de definitie voor een nanomateriaal, zoals gepubliceerd in de
Aanbeveling voor de definitie van een nanomateriaal (Aanbeveling
2011/696/EU). De Europese Commissie wil de definitie in de
Cosmeticaverordening nu aanpassen aan de definitie uit de
Aanbeveling. Deze aangepaste definitie zou dan gereed moeten zijn
in juli 2013, tegelijk met het van kracht worden van de
nano-specifieke vereisten van de Cosmeticaverordening.
De Europese Consumenten
Organisatie BEUC heeft onlangs een standpunt geformuleerd naar
aanleiding van deze ontwikkelingen. BEUC benoemt een aantal
aspecten die volgens hen in een dergelijke definitie thuishoren om
de consument optimaal te beschermen tegen de onbekende gevaren van
nanodeeltjes in cosmetische producten. Het gaat om de volgende
elementen:
- het betreft alle materialen waarin meer dan 0,15% van het aantal deeltjes aanwezig is in de nanoschaal;
- bijproducten die niet met opzet zijn geproduceerd, maar wel op nanoschaal aanwezig zijn, worden meegenomen;
- oplosbare nanodeeltjes en nanostructuren worden meegenomen, als deze specifiek zijn ontworpen om ingekapselde stoffen te vervoeren en vrij te laten komen in de systemische circulatie;
- speciale nanodeeltjes die kleiner zijn dan 1 nanometer, zoals fullerenen, worden meegenomen;
een nieuw criterium voor het volumespecifieke oppervlakte moet
worden toegevoegd, omdat de deeltjesgrootteverdeling alleen niet
voldoende is om informatie over oppervlakte te geven die
gerelateerd is aan de reactiviteit van de deeltjes.
RIVM/KIR overweging: De Europese
aanbeveling voor de definitie van nanomaterialen is zeer algemeen
opgesteld. De definitie dient voor verschillende wettelijke kaders
nog te worden ingevuld door het opstellen van specifieke eisen
(zie
in deze signaleringsbrief). Dit speelt nu onder meer voor
cosmetica. DG (directeur-generaal) SANCO (Directoraat Generaal Gezondheid en Consumenten
– Santé et Consommateurs) heeft een werkgroep ingesteld met
vertegenwoordigers van alle stakeholders (industrie, EU-lidstaten,
consumentenorganisaties en Europese Commissie) om de definitie in
de Cosmeticaverordening verder te specificeren. BEUC neemt ook deel
aan deze werkgroep. De belangrijkste aanpassing die BEUC voorstelt
is de verlaging van de grens van het aantal deeltjes om materiaal
het ‘nano’-stempel te geven. BEUC wil deze grens van 50% (zoals
opgenomen in de Aanbeveling) naar 0,15% verlagen voor ingrediënten
in cosmetica. Op deze manier wil BEUC meer consumenten beschermen.
De DG SANCO werkgroep bediscussieert op dit moment een verlaging
van 50% naar 10%.
Volgens het RIVM zijn er twee redeneringen mogelijk om af te wijken
van de 50%:
- verbetering van het inzicht in de risico’s van het gebruik van cosmetica die nanomaterialen bevatten of verbetering van de bescherming van de consument;
- verbetering van de traceerbaarheid (beschikbaarheid van informatie) en transparantie (‘recht op informatie’) voor de consument en ten behoeve van (handhaving) van regelgeving.
De aanbeveling voor de definitie van nanomaterialen van de EC
geeft echter geen basis voor het verlagen van het percentage met de
argumentatie van traceerbaarheid of transparantie.
Een verlaging van de drempelwaarde, naar 10 % of naar de door BEUC
voorgestelde grens van 0,15%, betekent dat meer cosmeticaproducten
als ‘nano’ worden geïdentificeerd. Hoewel dit gepaard gaat met een
toename aan beschikbare informatie over cosmetica die
nanomaterialen bevatten, kan er niet gesproken worden over een
betere bescherming van de consument bij een lager percentage. Het
percentage van het aantal nanodeeltjes (50%, 10% of 0,15%) zegt nl.
niets over het risico van het cosmetische product waar het
nanomateriaal als ingrediënt in verwerkt is.
Een afwijking van het percentage van 50% kan leiden tot
discrepantie tussen de wetgevende kaders (bv. voeding en cosmetica)
en daarmee verwarring bij de consument en stakeholders veroorzaken.
Het RIVM ziet om de hierboven genoemde redenen op dit moment geen
aanleiding om van het percentage van 50 % af te wijken.
Beleidsontwikkelingen in Verenigde Staten
Net als de EU, zoeken ook de Verenigde Staten naar passende wet-
en regelgeving om risico’s van nanomaterialen te kunnen beheersen.
Complicerende factor zijn de vele hiaten in de huidige kennis over
risico’s voor mens en milieu. Een recente publicatie
uit de VS beschrijft de reikwijdte van bestaande wetgeving om de
veiligheid van nanomaterialen voor mens en milieu te garanderen. De
‘US Toxic Substances
Control Act’ (TSCA) geldt als ‘basis’-wetgeving, die in Amerika
nanomaterialen reguleert op federaal niveau. Verdere
beleidsontwikkeling valt of staat voor een belangrijk deel met het
beschikbaar komen van de juiste informatie. Via het Amerikaanse
nanomateriaalregister
verschijnen inmiddels online steeds meer gegevens over
karakteristieken van bekende nanomaterialen. Gerenommeerde
instituten als het Research Triangle Institute (RTI) en
National
Institute of Environmental Health Sciences (NIEHS) zijn hierbij
betrokken. De site is vooral bedoeld voor wetenschappers, maar is
gratis toegankelijk voor iedereen.
RIVM/KIR-overweging: Opvallend
aspect is dat in de VS specifieke aandacht uitgaat naar de private
sector om juist daar voldoende deskundigheid te krijgen voor
risicoreductie, ook al zijn er nog onvoldoende duidelijke bewijzen
van risico’s. Het artikel
beschrijft verder dat vernieuwingen binnen TSCA om de hiaten op het
gebied van nanomaterialen aan te pakken vastlopen in het
Amerikaanse congres. De benadering van de ‘Massachusetts Toxics
Use Reduction Act’ (TURA), een ‘state law’, wordt gezien als
een mechanisme om wel voortgang te boeken, in tegenstelling tot de
federale TSCA-wetgeving. Deze ontwikkeling is vergelijkbaar met de
ontwikkelingen in de EU. Afzonderlijke EU lidstaten proberen om –
sneller dan nu gaande is op EU-niveau – meer sturing en invulling
te geven aan de regulering van de veiligheid van nanomaterialen in
hun land. Het Amerikaanse artikel eindigt dat op ‘state level’ wel
belangrijke voordelen te boeken zijn, maar dat deze over het
algemeen toch beperkt blijven. Ook hier lijkt de parallel met de EU
aanwezig. Nationale activiteiten zijn belangrijk en werken
(hopelijk) ‘aanjagend’ richting EU, maar de meeste slagkracht gaat
vooralsnog toch uit van de Europese wet- en regelgeving.
Het Amerikaanse nanomateriaalregister
richt zich hoofdzakelijk op de fysische en chemische eigenschappen
van de nanomaterialen. Zo is het mogelijk om sneller en beter de
mogelijke effecten van (nieuwe) nanomaterialen op biologische
weefsels te kunnen inschatten. Onderzoekers zullen echter zelf nog
de gezondheidskundige aspecten moeten bepalen. De OESO verzamelt
vergelijkbare data in het Sponsorprogramma van de
Working Party on Manufactured Nanomaterials (WPMN). Deze
gegevens zijn echter slechts toegankelijk voor hen die aan een
bepaald materiaal in het Sponsorprogramma werken.
Vertering van nanomaterialen en ontstaan ziektes
Een cel kan materiaal van buiten de cel opnemen (‘endocytose’).
Een voorbeeld hiervan is een macrofaag in de long die, na
inademing, bijvoorbeeld bacteriën of nanodeeltjes, opneemt. Het
materiaal wordt tijdens de opname omgeven door een membraan, zodat
er blaasjes ontstaan. Deze blaasjes smelten samen met lysosomen.
Lysosomen zijn onderdelen van de cel die een hoge zuurgraad hebben
en waarin zich verteringsenzymen bevinden. Vervolgens vindt er
vertering van het materiaal plaats. De verteringsproducten komen
weer beschikbaar als bouwstenen voor de cel.
In het geval van biopersistente nanomaterialen kan dit proces
verstoord raken. Amerikaanse onderzoekers beschrijven in een recent
overzichtsartikel
wat er gebeurt als nanomaterialen slecht worden verteerd door een
cel. Dit wordt als een steeds belangrijker mechanisme gezien om
gezondheidschade door nanomaterialen te verklaren.
Naast materiaal van buiten de cel, verteert een cel ook materiaal
van binnen de cel. Dit kan lichaamseigen materiaal zijn,
bijvoorbeeld beschadigde eiwitten, maar ook bacteriën of
nanodeeltjes die de cel zijn binnengedrongen en niet omgeven zijn
door een membraan. Dit wordt autofagie genoemd en is belangrijk om
evenwicht in de cel te handhaven. Bij dit proces smelt het
autofagosoom (autofagie-blaasje omgeven door membraan) samen met
het lysosoom, waarna de inhoud wordt verteerd.
Nanomaterialen kunnen een nadelige invloed uitoefenen op deze
verteringsprocessen. Hiervoor zijn meerdere aangrijpingspunten:
1) nanomaterialen kunnen het samensmelten van het fagosoom met het
lysosoom blokkeren. Hierdoor breekt de inhoud niet meer af;
2) positief geladen nanomaterialen, bijvoorbeeld met aminegroepen,
kunnen het membraan van het lysosoom lek maken. Het lysosoom kan
vervolgens ‘zijn werk niet meer doen’;
3) nanomaterialen genereren oxidatieve stress en reactieve zuurstof
wat schade kan geven aan biomoleculen;
4) door nanomaterialen worden de lysosomen minder zuur waardoor de
vertering minder goed verloopt.
Uiteindelijk leiden al deze mechanismen tot celdood.
KIR/RIVM overweging: Bovenstaande
mechanismen zijn belangrijk voor de verklaring van de
schadelijkheid van sommige nanomaterialen. Deze processen spelen
vaak ook een rol bij verschillende aandoeningen, zoals lysosomale
stapelingsziekten, chronische ontsteking of neurodegeneratieve
aandoeningen. Bij neurodegeneratieve aandoeningen worden
ziekte-geassocieerde eiwitten niet goed afgebroken. Een voorbeeld
hiervan is amyloid-beta bij de ziekte van Alzheimer. Op dit moment
formuleren wetenschappers onderzoekshypotheses om de betrokkenheid
van nanomaterialen bij het ontstaan van deze ziekten na te gaan.
Het leggen van eventuele causale verbanden zal naar verwachting nog
een aantal jaren onderzoek vergen.
Naast deeltjes en vezels, nu ook “nanostrookjes”
De stroom aan het op de markt komen van verschillende typen nanomaterialen gaat gestaag door. De nieuwe materialen worden ook steeds vaker onderzocht op schadelijkheid en beschreven in de wetenschappelijke literatuur. Aanvankelijk ging de aandacht vooral uit naar de bolvormige nanomaterialen. Later kwamen vezels, waaronder koolstofnanobuisjes, in het vizier. Recent verscheen een onderzoek van het US National Institute for Occupational Safety and Health (NIOSH) over zogenaamde ‘nanobelts’, vrij vertaald in ‘nanostrookjes’ van titanium dioxide (TiO2). Deze hebben, bijvoorbeeld, een grotere fotokatalytische activiteit in zonnepanelen dan de bolvormige structuren.
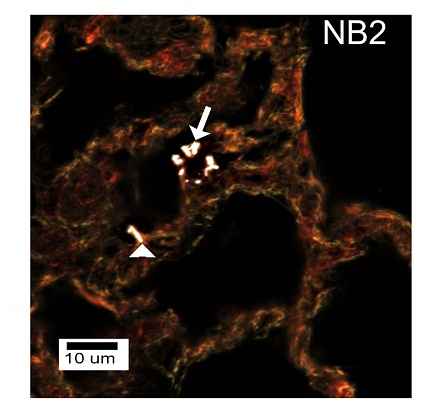
Links: een voorbeeld van nanostrookjes. Rechts: nanostrookjes aangetoond in longweefsel. Onder: nanostrookjes in long macrofagen. (Bron: Toxicological Sciences).
De onderzoekers vergeleken in muizen de effecten in de longen na
blootstelling aan bolvormige deeltjes en twee typen lange en korte
‘strookjes’ TiO2. Direct na de een eenmalige toediening waren alle
vormen van TiO2 in longmacrofagen terug te vinden. Alleen de
‘strookjes’ werden ook tussen de epitheelcellen gezien. Van deze
‘strookjes’ was bovendien alleen de lange vorm nog tussen de cellen
en naast de lymfe-afvoergangen waarneembaar. De korte vorm en de
bolvormige TiO2-nanomaterialen werden niet meer teruggevonden en
zijn blijkbaar afgevoerd door het lichaam, onder meer via de
lymfegangen. Het gevolg was dat de bolletjes nagenoeg geen nadelige
effecten in de longen veroorzaakten, terwijl de korte strookjes
duidelijk minder toxisch waren dan de lange.
RIVM/KIR-overweging: Dit is een
gedegen studie waarbij de nanomaterialen zorgvuldig zijn
gekarakteriseerd en ook de aanwezigheid in de longen is aangetoond.
De onderzoekers concluderen terecht dat ook hier de wetmatigheid
geldt dat onbuigzame en relatief lange nanomaterialen meer toxisch
zijn dan de kortere vorm of bolvormige deeltjes. Deze studie laat
zien dat de fysische aspecten een belangrijke factor zijn bij de
risicoschatting van nanomaterialen.
Download
- beleidsontw_VS.pdf
- database_consumenten_prod.pdf
- europ_regulatory_review.pdf
- inademen nano cosm_product.pdf
- milieueffecten_zinkoxide.pdf
- nano_huisvuilverbrandinginstall.pdf
- nanocentre.pdf
- nanomedicine.pdf
- nanostrookjes.pdf
- verantwoord gebruik nanomaterialen.pdf
- vertering nanomateriaal.pdf
- risicobeoord_nano_cosm_europ
- SCCS_opinie
- oplosbaarheid nano en gevolgen tox
- europ_consumentorg_nanodef.pdf