Steeds meer bacteriën ontwikkelen resistentie tegen antibiotica. Dat betekent dat sommige infecties slecht of, in sommige gevallen, helemaal niet meer kunnen worden behandeld. Deze mondiale dreiging heeft de laatste jaren steeds meer aandacht gekregen. In Nederland komen relatief weinig resistente bacteriën voor. Maar om ervoor te zorgen dat dit zo blijft, is ook in Nederland voor een landelijke aanpak gekozen Doel is om de sterfte en ziektelast ten gevolge van resistentie laag te houden, ook al neemt die in het buitenland toe. Voormalig minister Schippers van Volksgezondheid, Welzijn en Sport (VWS) heeft deze aanpak in 2015 door middel van een brief met de Tweede Kamer gedeeld. De aanpak richt zich op alle terreinen waar de gezondheid van mensen wordt bedreigd door antibioticaresistente bacteriën: zorg, dieren, voedsel en milieu. Dit noemen we de One-Health-benadering. In dit artikel richten we ons op 2 grote activiteiten in de zorg: intensivering van surveillance en het opzetten van zorgnetwerken. Surveillance wordt gebruikt om resistente bacteriën tijdig op te sporen en om het vóórkomen ervan te monitoren. Op deze manier kunnen trends zichtbaar gemaakt worden om tijdig interventies te kunnen plegen. Zorgnetwerken hebben tot doel ketenzorg te faciliteren. Bacteriën kennen geen grenzen tussen eerstelijns- en tweedelijnszorg. De bestrijding van antibioticaresistentie moet door samenwerking tussen zorginstellingen verbeteren en de zorgnetwerken hebben tot taak die samenwerking te bevorderen.
ib november 2017
Auteurs: A. Schreijer, K. Damen ,A. Reusken, C. Laurent, J. van der Gaag, S. de Greeff, M. van der Lubben, M. Mennen, M. Bonten
Infectieziekten Bulletin, jaargang 28, nummer 9, november 2017
Uitzonderingspositie
Antibioticaresistentie vormt in Nederland nog maar een beperkte bedreiging voor de volksgezondheid. In de resistentiewereld heeft ons land daardoor een uitzonderingspositie. Deze wordt toegeschreven aan het beperkte gebruik en de verstandige inzet van antibiotica, met name door huisartsen, goede infectiepreventie in ziekenhuizen en de landelijke surveillance van zorginfecties en (bijzonder resistente micro-organismen). Antibiotica resistentie is echter een snel groeiend wereldwijd probleem. In Europa gaat het daarbij vooral over de Zuid-Europese landen. Omdat wij leven in een wereld waar veel gereisd wordt zullen vroeg of laat ook in ons land antibioticaresistente bacteriën geïntroduceerd worden die wij niet of nauwelijks kennen. Die komen binnen met bijvoorbeeld gerepatrieerde patiënten, reizigers, oppervlaktewater, geïmporteerde dieren of voedsel. Om die dreiging ook in de toekomst het hoofd te kunnen bieden introduceerde minister Schippers van (Ministerie van Volksgezondheid, Welzijn en Sport) in 2015 een ambitieus beleidsplan (1), met daarin 3 concrete doelstellingen:
- het verminderen van het aantal dragers, infecties en sterftegevallen ten gevolge van BRMO;
- een 50% reductie van onjuist voorgeschreven antibiotica;
- een 50% reductie van vermijdbare zorggerelateerde infecties.
Zowel de intensivering van surveillance als het inrichten van zorgnetwerken moeten bijdragen aan de realisatie van deze doelen.
Zorgnetwerken
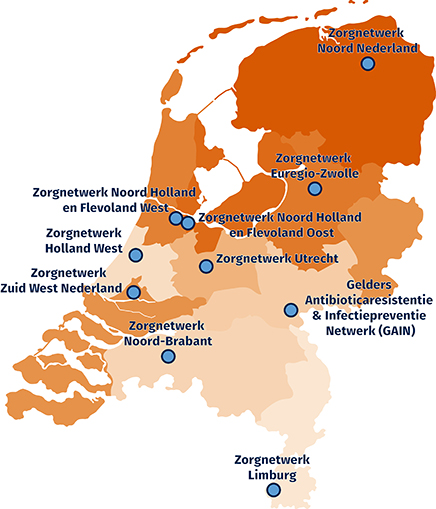
In Nederland worden 10 Regionale Zorgnetwerken (antibioticaresistentie) ingericht waarbinnen partijen in de gezondheidszorg met elkaar samenwerken (Figuur 1). In 2017 zijn de zorgnetwerken van start gegaan met de uitvoering van hun taken. Dat gebeurt in een pilotfase. De activiteiten binnen de Regionale Zorgnetwerken ABR moeten bijdragen aan de realisatie van de 6 doelstellingen zoals benoemd in de kamerbrief uit 2015 (Figuur 2). Het Landelijk Netwerk Acute Zorg (LNAZ) en (Gemeentelijke / Gemeenschappelijke GezondheidsDienst – Geneeskundige HulpverleningsOrganisatie in de Regio) ondersteunen en adviseren de zorgnetwerken tijdens deze pilotfase.
Figuur 1 De 10 regionale zorgnetwerken ABR.
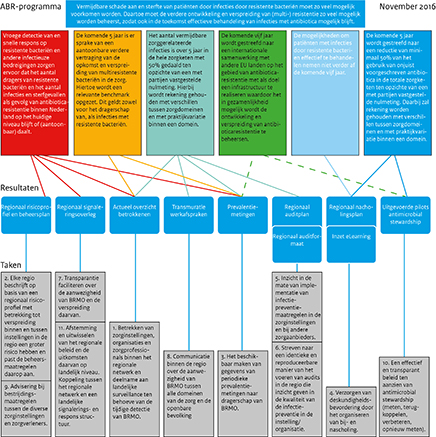
Figuur 2 De 6 doelstellingen zoals benoemd in de kamerbrief uit 2015.
Een regionale aanpak
Patiënten bewegen zich tussen verschillende zorginstellingen en zorgaanbieders in de regio. Resistente bacteriën bewegen met deze patiënten mee. Hierbij bestaat de kans op overdracht. Antibioticaresistentie blijft daarmee niet beperkt tot 1persoon of zorginstelling. Een aanpak op regionaal niveau en samenwerking die de verschillende domeinen overstijgt, maken de preventie en bestrijding van resistente bacteriën effectiever. Professionals in de cure, care en publieke gezondheid moeten daarom regionaal gezamenlijk werken aan een oplossing. Dit betekent dat ziekenhuizen, (Gemeentelijke Gezondheidsdienst)’en, microbiologische laboratoria, huisartsen, revalidatieklinieken, verpleeghuizen, instellingen voor verstandelijk gehandicapten en ambulante thuiszorginstellingen regionaal in een Zorgnetwerk ABR moeten samenwerken. Het doel van deze zorgnetwerken is antibioticaresistentie zoveel mogelijk te voorkomen en de verspreiding op regionaal niveau te bestrijden.
Inrichting van de Regionale Zorgnetwerken ABR
In elk zorgnetwerk is een ziekenhuis aangewezen dat alle relevante partijen (cure, care en publieke gezondheid) bij elkaar brengt in een stuurgroep. Deze regionale stuurgroep zet een regionaal coördinatieteam op voor de uitvoering en coördinatie van de taken van het Regionale Zorgnetwerk ABR. Dit team bestaat uit verschillende professionals: een arts-microbioloog, arts maatschappij en gezondheid, deskundige infectiepreventie, internist-infectioloog, specialist ouderengeneeskunde, huisarts en datamanager en/of epidemioloog. In elke regio neemt een kwartiermaker het voortouw in het opzetten van het zorgnetwerk.
Taken van de Zorgnetwerken ABR
De taken van de zorgnetwerken zijn door partijen in de zorg geformuleerd en beschreven in een functieprofiel (Zie tekst in kader) Binnen de zorgnetwerken blijven instellingen en professionals zelf verantwoordelijk voor de kwaliteit van zorg binnen de instelling. De taken van de zorgnetwerken zijn dus een aanvulling.
Een van de taken van de zorgnetwerken is het betrekken van zorginstellingen, organisaties en zorgprofessionals binnen het regionale netwerk en deelname aan landelijke surveillance ten behoeve van de tijdige detectie van BRMO (bijzonder resistente micro-organismen). Het welslagen van de zorgnetwerken vereist dat al deze partijen en zorgprofessionals betrokken worden en zich betrokken voelen bij het zorgnetwerk. Zij moeten immers gezamenlijk werken aan de realisatie van de eerder genoemde 6 doelstellingen, door deelname aan de activiteiten van het netwerk.
Andere taken van het zorgnetwerk zijn bijvoorbeeld het verzorgen van deskundigheidsbevordering op het gebied van de bestrijding van ABR, zoals infectiepreventie. Concreet voorbeeld is het organiseren van audits om inzicht te krijgen in de mate waarin instellingen infectiepreventiebeleid hebben geïmplementeerd. Ook moeten de netwerken gegevens van periodieke prevalentiemetingen naar dragerschap van BRMO beschikbaar gaan maken.
Deelname aan het zorgnetwerk vraagt een inspanning van de betrokken organisaties, instellingen en zorgprofessionals, maar het zorgnetwerk levert hen ook veel op. Een grote meerwaarde van het zorgnetwerk is dat verheffingen van BRMO binnen de regio sneller gesignaleerd kunnen worden, zodat instellingen op tijd hun bestrijdingsmaatregelen kunnen treffen. Ook ontstaat er binnen de regio meer samenhang in het infectiepreventiebeleid, wat individuele instellingen ten goede komt omdat er vanuit de regio minder overdracht van resistente bacteriën zal zijn.
Voor de pilotperiode hebben de zorgnetwerken per taak afspraken gemaakt, die zijn afgeleid van de eerdergenoemde 6 doelstellingen van het ABR-programma (Figuur 2). Hierbij gaat het bijvoorbeeld om het opstellen van een regionaal risicoprofiel en beheersplan op basis van de gesignaleerde risico’s, het opstellen van een actueel overzicht van betrokkenen en een regionaal audit- en nascholingsplan.
Pilotperiode
Onder coördinatie van de kwartiermakers zijn de zorgnetwerken gestart met de uitvoering van hun taken. Dat gebeurt in een pilot met subsidie van VWS. Deze pilot loopt tot mei 2019. In deze pilotfase beschrijven de zorgnetwerken hun best practices en delen zij deze met de andere regio’s. Daarnaast doen zij, in afstemming met elkaar, aanbevelingen aan VWS, die het toekomstig beleid voor de zorgnetwerken formuleert. Het accent in de uitvoering ligt in 2017 op het inrichten van de organisatie van de zorgnetwerken en inhoudelijke voorbereiding van de activiteiten.
Aanvullende subsidie
Zorgnetwerken kunnen, evenals regionale partijen/professionals (via het zorgnetwerk) tijdens de pilotfase concrete voorstellen doen voor nieuwe activiteiten, . en hiervoor bepaalde onder voorwaarden een subsidie krijgen van het ministerie van VWS.
Surveillance
Surveillance van infectieziekten is het zo systematisch mogelijk verzamelen van relevante gegevens over infectieziekten. Deze gegevens kunnen lokaal, regionaal en nationaal de infectieziektebestrijding en bestrijding van antibioticaresistentie ondersteunen. Bestrijding omvat tal van maatregelen. Denk daarbij aan zowel de behandeling van ziekten, de preventie van verspreiding en bepalen van risicofactoren voor ziekte. Surveillancegegevens zijn vaak de basis om het beleid te bepalen. Het gaat hier om bijvoorbeeld surveillance van zorginfecties en (Antimicrobial Resistance). (1,2) Tijdig kunnen ingrijpen is hierbij het hoofddoel.
Gebruik maken van al bestaande gegevens over bijvoorbeeld uitslagen van individuele patiëntendiagnostiek voorkomt registratie- of werkdruk. Maar efficiënte en effectieve surveillance vraagt ook dat de gegevens volgens een vooraf goed doordachte manier structureel worden verzameld, geaggregeerd, geanalyseerd en (terug)gekoppeld. Hier zijn zowel technische - als juridische factoren (bijvoorbeeld eigenaarschap) mee gemoeid waardoor er aanvullende en soms ook andere eisen aan de gegevens worden gesteld dan in het geval van registratie voor individuele patiëntdiagnostiek of kwaliteitsdoeleinden.
Surveillancegegevens kunnen gebruikt worden om vragen te beantwoorden die op lokaal, regionaal of landelijk niveau spelen. Men wil bijvoorbeeld weten of een bepaalde regionale verheffing daadwerkelijk een verheffing is en hoe deze kan worden verklaard. Aan de hand van surveillancegegevens kan worden bepaald of er sprake is van transmissie en of er aanvullende acties noodzakelijk zijn op regionaal niveau. Daarnaast komen er specifieke vragen op landelijk niveau voor: Hoe groot is dit probleem en is er sprake van een regio-overstijgende dreiging? Is er een noodzaak richtlijnen aan te passen? Is iedereen op de hoogte voor wie dit relevant is?
Het antwoord op de vraag of surveillance decentraal of centraal moet gebeuren is simpel: allebei. Daarom moeten we er voor zorgen dat het genereren, verzamelen, integreren en interpreteren van gegevens leidt tot zowel lokale-, regionale- als nationale inzichten, op basis waarvan op elk niveau specifieke acties genomen kunnen worden. Dezelfde gegevens kunnen dan niet alleen het individuele patiëntbelang, maar ook het publieke belang van surveillance en het professionele en institutionele belang van kwaliteitsborging, ondersteunen.
De (verbeterde) landelijke surveillance ABR steunt op 3 pijlers:
Surveillance van resistente bacteriën
De eerste pijler is de surveillance van het aantal dragers, infecties en sterftegevallen ten gevolge van BRMO. Hierbij wordt voortgebouwd op bestaande surveillancesystemen, zoals ISIS-AR, TypeNed en het maanelijkse Signaleringsoverleg Ziekenhuisinfecties & Antimicrobiële resistentie (SOZI/AMR). Uitslagen van Nederlandse Medisch Microbiologische Laboratoria (MML) worden sinds 2008 centraal verzameld in het ISIS-AR systeem. Op dit moment is 75% van de (medisch microbiologisch laboratorium)’s aangesloten en in 2018 zal dit voor alle Nederlandse MML’s gelden. Daarmee is er een compleet overzicht van alle BRMO’s (en ook niet-BRMO’s) in Nederland afkomstig van patiënten waarbij microbiologische diagnostiek verricht is. Koppeling van al die gegevens is nog een uitdaging omdat MML’s verschillende laboratoriumsystemen hebben en uitslagen op verschillende wijze coderen. Een cruciaal onderdeel van de vernieuwde surveillance is landelijke afstemming over uniforme codering van uitslagen (Eenheid van Taal), waardoor tijdrovende en foutgevoelige hercodering overbodig wordt. Hierdoor is de gemiddelde “doorschiettijd” (van MML naar ISIS-AR) op dit moment nog 6 maanden. Het streven is om dit terug te brengen naar maximaal enkele weken, zodat de gegevenscollectie ook actueel is. Aan de pilot Eenheid van Taal, die in is 2016 gestart, doen 5 MML’s en een aantal bouwers van laboratoriumsystemen mee. Het streven is om in 2018 de andere MML’s te betrekken.
Daarnaast wordt de surveillance van bijzonder resistente micro-organismen uitgebreid. Al 25 jaar worden alle methicillineresistente Staphylococcus aureus (MRSA) isolaten door MML’s naar het RIVM gestuurd voor typering. Met zulke informatie zijn veranderingen in de moleculaire epidemiologie en ongemerkte verspreiding vast te stellen. Mede hierdoor konden de opkomst en verspreiding van de veegerelateerde (Methicilline-resistente Staphylococcus aureus) in een vroeg stadium herkend worden. Het RIVM is ook het landelijke referentiecentrum voor carbapenemaseproducerende Enterobacteriaceae (zoals Klebsiella pneumoniae en Escherichia coli), afgekort als (Carbapenemase-producerende Enterobacterales). Ook voor andere relevante BRMO zal een vorm van landelijke surveillance opgezet worden. Gekoppeld aan de isolaten worden epidemiologische gegevens van dragers verzameld, zodat risicogroepen en risicofactoren kunnen worden vastgesteld. Die kennis kan dan weer gebruikt worden om, bijvoorbeeld, screening bij ziekenhuisopname uit te voeren (of af te schaffen). Omdat er relatief weinig bekend is over de mate van dragerschap met BRMO in verpleeghuizen zal de prevalentie van (Extended spectrum beta-lactamases)-producerende bacteriën en CPE begin 2018 met een grootschalig landelijk puntprevalentie onderzoek worden vastgesteld. Het plan is om in elk van de 10 zorgnetwerken minimaal 40 bewoners van minimaal 30 verpleeghuizen eenmalig op dragerschap met ESBL-producerende bacteriën te onderzoeken.
Surveillance zorggerelateerde infecties
De tweede pijler is de surveillance van zorggerelateerde infecties, zoals post-operatieve wondinfecties na knie- of heupprothesechirurgie. Hiervoor zal het bestaande PREZIES-systeem aangepast worden. Het huidige systeem wordt door velen als te arbeidsintensief ervaren en heeft veel subjectieve componenten, die de betrouwbaarheid niet ten goede komen. De aanwezigheid van elektronische patiëntdossiers maakt het mogelijk de registratielast door automatisering substantieel te verminderen. En door alleen gebruik te maken van objectief vast te stellen diagnostische criteria wordt de betrouwbaarheid van de registratie groter waardoor de resultaten zich beter lenen voor benchmarking. Als dat gerealiseerd is kan bepaald gaan worden welk deel van deze infecties vermijdbaar is en kan vastgesteld worden of bepaalde interventies daar invloed op hebben. Deze nieuwe aanpak zal als eerste voor postoperatieve wondinfecties na knie- of heupprothesechirurgie worden aangewend. De ontwikkelde methodologie zal in 2018 als pilot in verschillende ziekenhuizen worden geïmplementeerd.
Surveillance antibioticagebruik
De derde pijler bestaat uit de surveillance van antibioticagebruik. Het aantal kilo’s gebruikte antibiotica (bij mens en dier) wordt al elk jaar gerapporteerd in Nethmap en (Monitoring of antimicrobial resistance and antibiotic usage in animals in the Netherlands). (2) Voor humaan gebruik is het echter onbekend waarom de antibiotica gegeven worden, en die kennis is nodig om te kunnen beoordelen of het gebruik al dan niet onjuist is. Pilots worden opgezet om, wederom via automatisering, het gebruik te koppelen aan de indicaties, zowel in ziekenhuizen, verpleeghuizen als bij huisartsen. Via benchmarking en terugkoppeling kan op basis van deze surveillance aan antibiotic stewardship vorm gegeven worden, zoals dat nu al gebeurt bij huisartsen in diagnostische toetsoverleggen (DTO’s).
De vernieuwde landelijke surveillance bouwt nadrukkelijk voort op de reeds bestaande surveillance-instrumenten, die – vooral door buitenlandse collega’s – al als van hoge kwaliteit werden beschouwd. De gegevensverzameling van de surveillance vindt grotendeels in de zich ontwikkelende regionale zorgnetwerken plaats. Door de centrale aansturing zullen deze netwerken bijdragen aan een landelijk dekkend surveillancesysteem waarin voor het land en voor elke regio representatieve gegevens verkregen worden. Hiermee kunnen dan ook de verschillende activiteiten in en tussen de regio’s met elkaar vergeleken worden.
Taken zorgnetwerken
De zorgnetwerken hebben de volgende 11 taken:
- Het betrekken van zorginstellingen, organisaties en zorgprofessionals binnen het regionale netwerk en deelname aan landelijke surveillance.
- Het opstellen van een regionaal risicoprofiel met betrekking tot verspreiding binnen en tussen instellingen of er in de regio een groter risico is en het daarop aanpassen van de beheersmaatregelen.
- Het beschikbaar maken van gegevens van periodieke prevalentiemetingen naar dragerschap van BRMO.
- Deskundigheidsbevordering door het organiseren van bij- en nascholing van zorgprofessionals.
- Het verkrijgen van inzicht in de mate van implementatie van infectiepreventiemaatregelen in de zorginstellingen en bij andere zorgaanbieders.
- Het streven naar een identieke en reproduceerbare manier van het voeren van audits in de regio die inzicht geven in de kwaliteit van de infectiepreventie in de instelling/organisatie.
- Transparantie faciliteren en communicatie over de aanwezigheid van BRMO in de regio
- Advisering bij bestrijdingsmaatregelen.
- Een effectief en transparant beleid ten aanzien van antimicrobial stewardship.
- Afstemming en uitwisselen van het regionale beleid en de uitkomsten daarvan op landelijk niveau.
Auteurs
A. Schreijer1, K. Damen2,A. Reusken2, C. Laurent1, J. van der Gaag3, S. de Greeff4, M. van der Lubben4, M. Mennen4, M. Bonten5,
- GGD GHOR Nederland
- Landelijk Netwerk Acute Zorg
- Emeritus hoogleraar Radboud (Universitair Medisch Centrum), CPME Europese artsenorganisatie, Brussel
- Centrum Infectieziektebestrijding, RIVM
- Afdeling Medische microbiologie, Universiteit Utrecht
Correspondentie
marieken.van.der.lubben@rivm.nl
Literatuur
- Aanpak antibioticaresistentie, juni 2015, Ministerie van VWS, Den Haag. Voortgang aanpak antibioticaresistentie, 7 juli 2016, Ministerie van VWS, Den Haag.
- S.C. de Greefff, J.W. Mouton, (Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands) 2017: Consumption of antimicrobial agents and antimicrobial resistance among medically important bacteria in the Netherlands / MARAN 2017: Monitoring of antimicrobial resistance and antibiotic usage in animals in the Netherlands in 2016. RIVM Rapport 2017-0056, Bilthoven.