Infectieziekten Bulletin, maart 2024
Auteurs
C.E. van Ewijk1,2, A. Afrian1, N. M. van Sorge3, A. Steens1
- Centrum Infectieziektebestrijding, RIVM
- European Programme for Intervention Epidemiology Training (EPIET), European Centre for Disease Prevention and Control (ECDC), Solna, Sweden
- Amsterdam (Universitair Medisch Centrum)
Inleiding
Pneumokokken (Streptococcus pneumoniae) zijn Gram-positieve bacteriën die asymptomatisch de bovenste luchtwegen koloniseren.1 Pneumokokken kunnen echter ook invasieve pneumokkenziekte (IPD) veroorzaken, wat kan leiden tot ernstige ziekte of overlijden met name bij kinderen jonger dan 5 jaar en volwassenen van 60 jaar en ouder. De (invasieve pneumokokkenziekte)-incidentie stijgt met de leeftijd, vooral bij volwassenen van 60 jaar en ouder, vanwege een verminderde werking van het immuunsysteem.2 Bij volwassenen is S. pneumoniae één van de belangrijkste verwekkers van een pneumonie met een mortaliteit oplopend tot 40%.3 Er worden zo’n 100 pneumokokvarianten onderscheiden op basis van verschillen in kapselsamenstelling; deze varianten worden serotypen genoemd. De virulentie en de kans op het veroorzaken van een invasieve infectie is serotype-afhankelijk.4 Sinds 2006 worden kinderen tegen pneumokokken gevaccineerd om morbiditeit en mortaliteit als gevolg van IPD te reduceren; vanaf 2006 met het 7-valente pneumokok-conjugaat-vaccin (PCV7) en sinds 2011 met (Synflorix®). Naast een direct beschermend effect op het gevaccineerde kind, zorgen PCVs voor een indirect beschermend effect op mensen in de omgeving (groepsimmuniteit) doordat kolonisatie en daarmee de kans op transmissie via respiratoire druppels vermindert.5 Sinds de implementatie van kindervaccinatie is het aantal IPD-gevallen veroorzaakt door vaccin-gedekte serotypen zowel onder kinderen als volwassenen gedaald.6 7 Tegenwoordig krijgen vooral ouderen en individuen uit medische risicogroepen IPD veroorzaakt door niet-PCV10-serotypen.8 In 2018 adviseerde de Gezondheidsraad om volwassenen van 60 t/m 79 jaar 5-jaarlijks te vaccineren met het 23-valente pneumokokken polysaccharide-vaccin (PPV23).9 Dit vaccin beschermt alleen het gevaccineerde individu tegen IPD door 23 serotypen en heeft een geschatte effectiviteit van 32-64%.10 Pneumokokkenvaccinatie bij volwassenen is gestart in september 2020, waarbij de doelgroep gefaseerd werd uitgenodigd.
IPD bij kinderen geboren vanaf 2006 is meldingsplichtig (categorie C) sinds 2008. Deze meldplicht werd in april 2021 uitgebreid naar IPD bij volwassenen van 60 jaar en ouder, om de impact en effectiviteit van PPV23 te kunnen monitoren en de vaccinatiestrategie te informeren.
Invasieve pneumokokkenziekte surveillance
Het Rijkinstituut voor Volksgezondheid en Milieu (RIVM) is verantwoordelijk voor de landelijke IPD-surveillance, die gebaseerd is op epidemiologische surveillance van de regionale (Gemeentelijke Gezondheidsdienst)’en en laboratoriumsurveillance van het Nederlands Referentie Laboratorium voor Bacteriële Meningitis (NRLBM).12 De surveillance is gericht op de evaluatie van het vaccinatiebeleid en clusterdetectie. Een pneumokokkeninfectie is meldingsplichtig als de bacterie wordt aangetoond in lichaamsmateriaal dat normaal steriel is, zoals liquor, bloed, of pleuravocht. Behandelend artsen en laboratoria worden verzocht een patiënt met IPD binnen één werkdag na diagnose te melden aan de regionale GGD.13, 14 Daarnaast wordt aan het regionale laboratorium gevraagd het betreffende pneumokok-isolaat op te sturen naar het (Nederlands Referentie Laboratorium voor Bacteriële Meningitis) voor serotypering.
Na het ontvangen van een IPD-melding, neemt de GGD contact op met de behandelend arts en/of patiënt. Hierbij worden (epidemiologische) gegevens van de patiënt verzameld, zoals geslacht, leeftijd, viercijferige-postcode, eerste ziektedag, diagnosedatum, ziektebeeld, ziekenhuisopname, comorbiditeit en vaccinatiestatus.
De gegevens worden vervolgens binnen drie werkdagen gepseudonimiseerd gerapporteerd in het Osiris-informatiesysteem van het RIVM, waarbij het NRLBM-nummer (‘ons-nummer’) en serotype later worden aangevuld.13
Het NRLBM rapporteert isolaten waarbij serotypering is verricht maandelijks aan het RIVM. Hierbij worden gegevens verstrekt over het serotype, type materiaal waar de pneumokok uit is geïsoleerd met afname- en laboratoriumdatum, NRLBM-nummer, woonplaats, geboortedatum en ziektebeeld van patiënt (voor zover bekend). Het RIVM koppelt vervolgens de NRLBM-data en epidemiologische Osiris-data voor een volledige surveillance; eerst op basis van NRLBM-nummer, en indien dit niet mogelijk is, op andere variabelen waar mogelijk.
Doel van het onderzoek
Welk vaccin het meest geschikt is voor volwassenen hangt af van schattingen op basis van surveillancedata.11 Goede kwaliteit van surveillance data is daarvoor van belang. Wij evalueerden het IPD-surveillancesysteem voor volwassenen van 60 jaar en ouder, bijna een jaar na het uitbreiden van de IPD-meldplicht, op drie aspecten:
- Ontvangt het NRLBM alle isolaten van IPD in volwassenen van 60 jaar en ouder van alle medisch microbiologische laboratoria.
- Is er een bijbehorende melding in Osiris gemaakt.
- Zijn de epidemiologische gegevens van Osiris-meldingen volledig?
De resultaten werden teruggekoppeld naar de GGD’en, met als doel de surveillance te verbeteren.
Methode
Studie populatie
IPD-meldingen van volwassenen van 60 jaar en ouder met een pneumokok-isolaat in het NRLBM-bestand of een melding in Osiris van 1 april 2021 t/m 1 februari 2022. Osiris-data werden geëxtraheerd op 10 februari 2022.
Volledigheid NRLBM-meldingen
Om te beoordelen of het NRLBM alle IPD-isolaten ontving van de medisch microbiologische laboratoria, werd per laboratorium het aantal isolaten van het NRLBM vergeleken met het aantal isolaten in het Infectieziekten Surveillance Informatie Systeem-Antibiotica Resistentie (ISIS-AR), voor de periode 1 juli t/m 31 december 2021. Laboratoria die niet aan beide systemen rapporteerden in deze periode werden geëxcludeerd (n=14). We gebruikten (Infectious Disease Surveillance Information System for Antibiotic Resistance) als ‘gouden standaard’. ISIS-AR is een surveillancesysteem dat gepseudonimiseerde gegevens ontvangt van participerende laboratoria van alle antibiotica resistentiebepalingen, waaronder voor pneumokokken.15
Volledigheid Osiris-meldingen
We beoordeelden of aan elk NRLBM-isolaat een Osiris-melding te koppelen was in twee stappen. Als eerste probeerden we de isolaten te koppelen via NRLBM-nummer en geboortejaar. Indien koppeling via het NRLBM-nummer onmogelijk was vanwege een incorrect (een onjuist aantal cijfers of letters) of onbekend NRLBM-nummer in Osiris, vond koppeling plaats via een probabilistische methode op basis van geslacht, geboortejaar, meldingsjaar, diagnosedatum (Osiris) en diagnostiek afnamedatum (NRLBM), gemeentecode, en serotype. De probabilistische methode hield rekening met eventuele minimale afwijkingen in geboorte- afname- en/of diagnosedatum in beide databestanden. Koppelingen werden handmatig gecheckt en zo nodig aangepast (n=1). Als we geen koppeling konden maken, kon dat betekenen dat er geen Osiris-melding was gemaakt, of dat de Osiris-melding te weinig overeenkomstige informatie bevatte om een koppeling te maken met het NRLBM-bestand. De percentages IPD-meldingen van het totaal dat enkel in NRLBM, Osiris of in beide databestanden waren gemeld, werden berekend over het geheel, per GGD-regio, wel/niet vaccinatiedoelgroep, en wel/niet IPD door een serotype dat gedekt is door PPV23 (PPV23-serotype). Een patiënt behoorde tot de vaccinatiedoelgroep indien geboren in 1941 t/m 1947 (hele studie periode), of geboren in 1948 t/m 1952 met een diagnosedatum vanaf 1 november 2021.
Volledigheid epidemiologische gegevens
De volledigheid van epidemiologische gegevens van de Osiris-meldingen werd beoordeeld voor de variabelen zoals beschreven in Tabel 1. Deze werden gekozen vanwege hun belang voor een correcte koppeling aan een NRLBM-isolaat, of voor het berekenen van de impact en effectiviteit van PPV23.
Statistische analyse
Koppeling van Osiris- aan NRLBM-databestand en beschrijvende analyses werden verricht in R versie 4.0.2. Probabilistische koppeling werd gedaan middels het fastLink R-package.16 Percentages werden berekend van de gekoppelde en niet gekoppelde NRLBM- en Osiris-meldingen en van volledig ingevulde epidemiologische Osiris-variabelen.
Resultaten
Volledigheid NRLBM-meldingen
Zevenendertig laboratoria rapporteerden gedurende de studieperiode aan zowel NRLBM als ISIS-AR. In totaal werden 355 isolaten ingestuurd naar het NRLBM, en 370 isolaten werden gemeld aan ISIS-AR. Gebaseerd op deze aantallen werd geschat dat 96% van de pneumokok-isolaten door de diagnostische laboratoria naar het NRLBM zijn gestuurd.
Volledigheid Osiris-meldingen
Er werden 713 IPD-isolaten door het NRLBM en 619 IPD-meldingen door de GGD’en via Osiris gemeld aan het RIVM. Van de 713 NRLBM-isolaten konden er 567 (80%) gekoppeld worden aan een Osiris-melding: 346/567 (61%) op basis van NRLBM-nummer en geboortejaar, en 221/567 (39%) via de probabilistische methode. Er was geen verschil in de koppelingspercentages over tijd.
Van de NRLBM-meldingen van volwassenen die behoorden tot de vaccinatiedoelgroep kon 82% (154/188) worden gekoppeld, ten opzichte van 78% (413/525) van volwassenen die (nog) niet tot de vaccinatiedoelgroep behoorden. Van de NRLBM-meldingen waarbij IPD was veroorzaakt door PPV23-serotypen kon 82% (447/547) worden gekoppeld t.o.v. 72% (120/166) voor NRLBM-meldingen van IPD door niet-PPV23-serotypen.
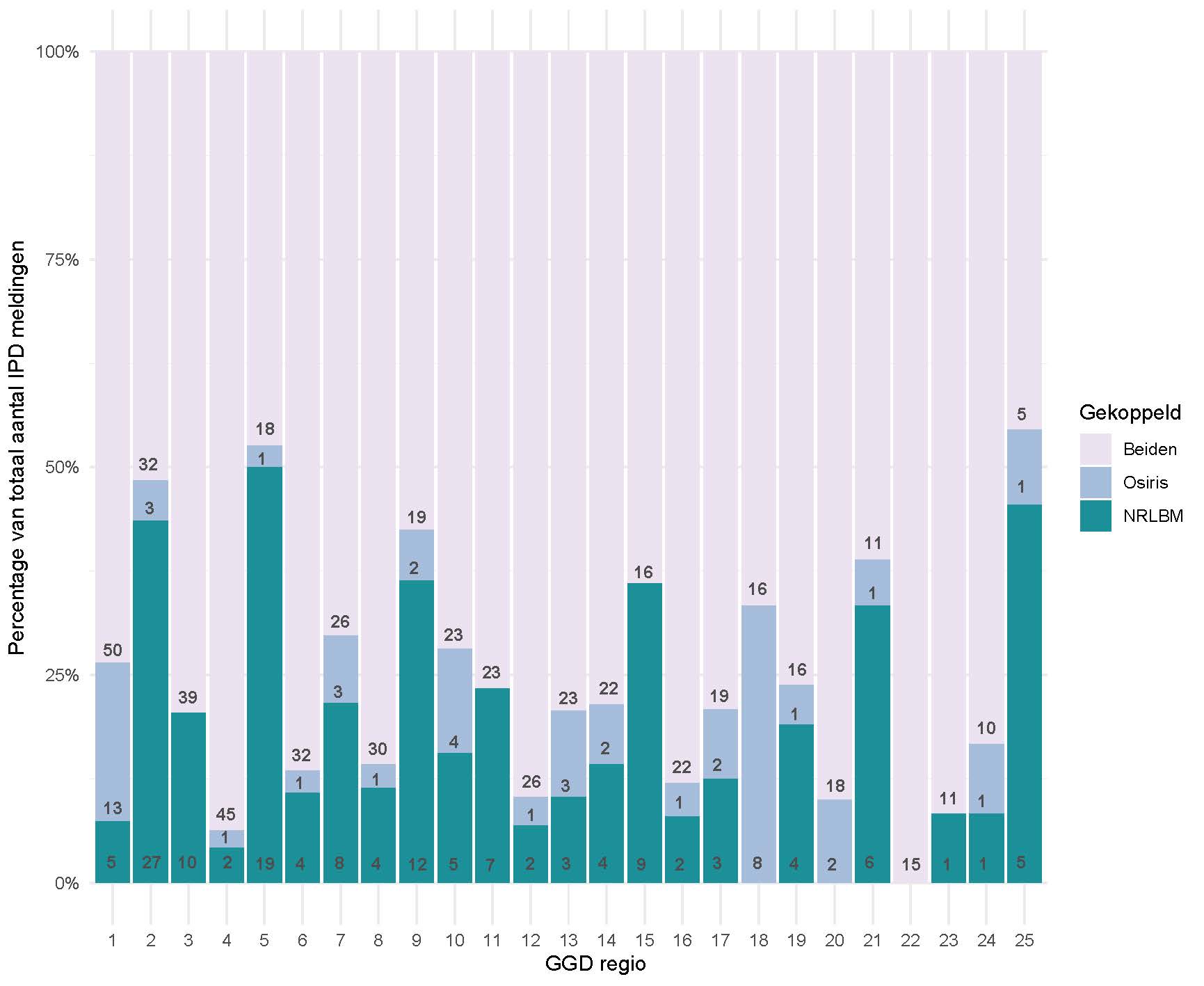
Het percentage NRLBM-meldingen dat niet gekoppeld kon worden, varieerde per GGD-regio tussen 0 en 50% van de NRLBM-meldingen (mediaan 5, range 0-27 meldingen) (zie Figuur 1)
Na de koppeling kon 8% (52/619) van de Osiris-meldingen niet gekoppeld worden aan een NRLBM-melding.
Zoals verwacht, was bij niet gekoppelde Osiris-meldingen het NRLBM-nummer vaker onbekend of incorrect (50/52, 96% t.o.v. 218/567, 38%) en de diagnosedatum onbekend (4/52 8% t.o.v. 8/567, 1%), vergeleken met gekoppelde Osiris-meldingen.
Figuur 1 – Het koppelingspercentage en absolute aantallen van IPD-gevallen in alleen (Nederlands Referentie Laboratorium voor Bacteriële Meningitis) of Osiris of beide databestanden van het totaal aantal IPD-meldingen per (Gemeentelijke Gezondheidsdienst) regio (Totaal=765: NRLBM gekoppeld n=567, NRLBM niet gekoppeld= 146, Osiris niet gekoppeld n=52), periode 1 april 2021 t/m 1 februari 2022.
Volledigheid epidemiologische gegevens
De volledigheid van epidemiologische gegevens in Osiris (N=619) was 92%-100% voor geslacht, geboortejaar, viercijferige postcode, ziektebeeld, diagnosedatum en overlijden. Vaccinatiestatus was ingevuld in 89% en serotype in 81% van de meldingen. Het (Nederlands Referentie Laboratorium voor Bacteriële Meningitis)-nummer was in 57% van de meldingen correct ingevuld. Vergeleken met volwassenen die (nog) niet tot de vaccinatiedoelgroep behoorden, was bij volwassenen behorende tot de vaccinatiedoelgroep het serotype (86% t.o.v. 79%) en het NRLBM-nummer (77% t.o.v. 50%) vaker (correct) ingevuld.
| Epidemiologische gegevens |
Osiris |
Vaccinatie |
(nog ) Geen vaccinatie doelgroep N-457 |
|||
|---|---|---|---|---|---|---|
| n | % | n | % | n | % | |
| Geslacht | 619 | 100 | 162 | 100 | 457 | 100 |
| Geboortejaar | 619 | 100 | 162 | 100 | 457 | 100 |
| Comorbiditeit * | 134 | 22 | 75 | 46 | 59 | 13 |
| Eerste ziektedag | 503 | 81 | 126 | 78 | 377 | 82 |
| Diagnose datum | 607 | 98 | 156 | 96 | 451 | 99 |
| Ziektebeeld | 613 | 99 | 159 | 98 | 454 | 99 |
| Overlijden | 571 | 92 | 149 | 92 | 422 | 92 |
| Indien overleden, overleden door (invasieve pneumokokkenziekte), n/N (%) | 37/49 | 7/10 | 30/39 | |||
| Vaccinatiestatus | 554 | 89 | 147 | 91 | 407 | 89 |
| Als gevaccineerd, aantal doses, n/N (%) | 61/72 | 85 | 50/59 | 85 | 11/13 | 85 |
| Als gevaccineerd, type vaccin, n/N (%) | 71/72 | 99 | 58/59 | 98 | 13/13 | 100 |
| Als gevaccineerd, datum laatste vaccinatie, n/N (%) | 61/72 | 85 | 50/59 | 85 | 11/13 | 85 |
| Serotype | 503 | 81 | 140 | 86 | 363 | 79 |
| (Nederlands Referentie Laboratorium voor Bacteriële Meningitis)-nummer | ||||||
| Incorrect nummer | 22 | 3 | 3 | 2 | 19 | 4 |
| Correct nummer | 351 | 57 | 125 | 77 | 226 | 50 |
| Onbekend | 246 | 40 | 34 | 21 | 212 | 46 |
| Viercijferige postcode | 615 | 99 | 160 | 99 | 455 | 99 |
* tot medio januari 2022 werd comorbiditeit enkel bij gevaccineerde patiënten uitgevraagd.
Beschouwing
Onze evaluatie van de (invasieve pneumokokkenziekte) surveillance bij volwassenen van 60 jaar en ouder laat zien dat regionale laboratoria adequaat pneumokok-isolaten insturen naar het (Nederlands Referentie Laboratorium voor Bacteriële Meningitis) voor serotypering; 96% van het aantal NRLBM-meldingen werd ook gerapporteerd in (Infectious Disease Surveillance Information System for Antibiotic Resistance). De koppeling van NRLBM-meldingen met Osiris-meldingen was met 80% minder succesvol. Dat gold in het bijzonder voor volwassenen die niet behoorden tot de vaccinatiegroep en/of IPD hadden die veroorzaakt werd door een niet-PPV23 serotype. Hieraan gerelateerd waren de epidemiologische gegevens, met name serotype en het NRLBM-nummer, voor volwassenen niet-behorend tot de vaccinatiedoelgroep vaker incompleet.
Er zijn verschillende potentiële oorzaken waardoor een koppeling niet gemaakt kan worden:
- Niet alle gevallen zijn gemeld aan de GGD of door de GGD in Osiris ingevoerd.
- Of er is een gebrek aan gegevens in de Osiris-melding waardoor de koppeling niet tot stand kan worden gebracht. De meest betrouwbare koppeling vindt plaats via het NRLBM-nummer, slechts 57% van alle Osiris-meldingen was correct gerapporteerd.
Voor een koppeling met de probabilistische methode zijn meerdere epidemiologische gegevens nodig in beide databestanden (geboortejaar, geslacht, meldingsjaar, viercijferige-postcode, diagnosedatum (Osiris) diagnostiek afnamedatum (NRLBM), serotype). Bij afwezigheid van het NRLBM-nummer en deze gegevens in het Osiris- en/of NRLBM-bestand zal koppeling niet mogelijk zijn.
Het verschil in het percentage dat gekoppeld kon worden tussen vaccinatiedoelgroep en niet-vaccinatiedoelgroep, en tussen PPV23- en niet-PPV23-serotypen kan op toeval berusten of een structurele oorzaak hebben, bijvoorbeeld als epidemiologische gegevens beter zijn ingevuld waardoor de kans op koppeling groter is. Een andere reden voor de selectieve koppeling kan ermee te maken hebben dat verschillende serotypen verschillende ziektebeelden kunnen veroorzaken.17 PPV23-infecties hebben mogelijk vaker een klassiek IPD-ziektebeeld waarbij pneumokokken uit het bloed of liquor geïsoleerd worden t.o.v. niet-PPV23-infecties. Alhoewel IPD waarbij pneumokokken uit andere normaal steriele plekken zijn geïsoleerd zoals uit pleuravocht en gewrichtspunctaat ook meldingsplichtig is, kan het zijn dat hiervoor de surveillance (nog) minder goed is.
Of de selectieve resultaten een structurele oorzaak hebben moet verder worden uitgezocht.
Selectieve koppeling van gevaccineerden/PPV23-serotypen kan gevolgen hebben voor het vaccinatiebeleid. Indien gevaccineerden/PPV23-serotypen vaker gemeld en/of gekoppeld worden, zal dit leiden tot een onderschatting van de vaccineffectiviteit. Ook zal de serotype-verdeling binnen subgroepen mogelijk niet representatief zijn, wat invloed heeft op de schattingen die gemaakt worden voor het percentage IPD dat door de verschillende vaccins gedekt kan worden. Deze schattingen zijn van groot belang voor de pneumokokkenvaccinkeuze voor ouderen, waarover de Gezondheidsraad recent nog advies heeft gegeven, en daarmee voor het landelijke preventiebeleid.18
Een volledige surveillance met zo volledig mogelijke epidemiologische data blijft dus relevant. Periodieke evaluatie van het surveillancesysteem met terugkoppeling naar betrokken partijen is hierbij essentieel. De resultaten van deze evaluatie werden teruggekoppeld middels presentaties en een factsheet naar de individuele GGD’en waar zo nodig verdere evaluatie van het interne surveillance systeem is of kan worden gestart.
Conclusie
Bijna alle isolaten van IPD-patiënten lijken ingestuurd te worden naar het NRLBM. Van de ingestuurde isolaten kon 80% gekoppeld worden aan een Osiris-melding. Een succesvolle koppeling leek tijdens de studieperiode samen te hangen met vaccinatiedoelgroep en serotype wat binnen subgroepen leidt tot een niet representatieve serotypeverdeling, en daarmee tot een onderschatting van de vaccineffectiviteit. Resultaten van deze periodieke evaluatie van het surveillancesysteem werden teruggekoppeld aan de individuele GGD’en. Een nieuwe evaluatie zal dit jaar plaatsvinden voor de periode 2022-2023.
Verantwoordingsnoot
Wij danken Wieke Altorf-van der Kuil en Annelot Schoffelen voor hun bijdrage aan de vergelijking tussen de aantallen van het (Nederlands Referentie Laboratorium voor Bacteriële Meningitis) en (Infectious Disease Surveillance Information System for Antibiotic Resistance). We danken de medisch microbiologische laboratoria voor het insturen van pneumokokkenisolaten en alle (Gemeentelijke Gezondheidsdienst)’en voor het melden van de (invasieve pneumokokkenziekte) gevallen. We danken Anneke Westerhof voor haar bijdrage aan pneumokokken surveillance.
- van Deursen AM, van den Bergh (antimicrobial resistance), Sanders EA. Carriage of Streptococcus pneumoniae in asymptomatic, community-dwelling elderly in the Netherlands. Vaccine. 2016;34(1):4-6.
- RIVM. Vaccinatiegraad en jaarverslag Rijksvaccinatieprogramma Nederland 2021. 2022.
- Jansen AGSC, Rodenburg (Gezondheidsdienst voor Dieren), de Greeff SC, Hak E, Veenhoven RH, Spanjaard L, et al. Invasive pneumococcal disease in the Netherlands: Syndromes, outcome and potential vaccine benefits. Vaccine. 2009;27(17):2394-401.
- Yildirim I, Hanage (work package), Lipsitch M, Shea KM, Stevenson A, Finkelstein J, et al. Serotype specific invasive capacity and persistent reduction in invasive pneumococcal disease. Vaccine. 2010;29(2):283-8.
- Spijkerman J, van Gils EJ, Veenhoven RH, Hak E, Yzerman EP, van der Ende A, et al. Carriage of Streptococcus pneumoniae 3 years after start of vaccination program, the Netherlands. Emerg Infect Dis. 2011;17(4):584-91.
- Rijksinstituut voor Volkgsezondheid en Milieu - Ministerie van Volksgezondheid WeS. Pneumokokkenziekte en vaccineren 2022 [01-06-2022]. Available from: https://rijksvaccinatieprogramma.nl/infectieziekten/pneumokokken.
- Peckeu L, van der Ende A, de Melker HE, Sanders (Environmental Assessment Module), Knol MJ. Impact and effectiveness of the 10-valent pneumococcal conjugate vaccine on invasive pneumococcal disease among children under 5 years of age in the Netherlands. Vaccine. 2021;39(2):431-7.
- Wagenvoort GH, Knol MJ, de Melker HE, Vlaminckx BJ, van der Ende A, Rozenbaum MH, et al. Risk and outcomes of invasive pneumococcal disease in adults with underlying conditions in the post-PCV7 era, The Netherlands. Vaccine. 2016;34(3):334-40.
- Gezondheidsraad. Vaccinatie van ouderen tegen pneumokokken. 2018.
- Winje BA BJ, Vestrheim (dengue fever), Denison E, Lepp T, Roth A, Valentiner-Branth P, Slotved HC, Storsæter J. Efficacy and effectiveness of pneumococcal vaccination in adults – a second update of the literature. Norwegian Institute for Public Health; 2022.
- RIVM. Pneumokokkenvaccinatie ouderen: informatie voor de Gezondheidsraad 2022 [Available from: https://www.rivm.nl/nieuws/pneumokokkenvaccinatie-ouderen-informatie-voor-gezondheidsraad.
- RIVM. Feiten en cijfers pneumokokkenziekte 2021 [Available from: https://www.rivm.nl/pneumokokken/professionals/feiten-en-cijfers-pneumokokkenziekte.
- Rijksinstituut voor Volkgsezondheid en Milieu - Ministerie van Volksgezondheid WeS. Pneumokokkenziekte 2019 [updated 2021. Available from: https://lci.rivm.nl/richtlijnen/pneumokokkenziekte.
- Wet publieke gezondheid, (2022).
- RIVM. Infectieziekten Surveillance Informatie Systeem-Antibiotica Resistentie 2021 [Available from: https://www.rivm.nl/isis-ar.
- Enamorado T. fastLink-package: Fast Probabilistic Record Linkage with Missing Data [Available from: https://rdrr.io/cran/fastLink/man/fastLink-package.html.
- Wagenvoort GH, Sanders EA, Vlaminckx BJ, Elberse KE, de Melker HE, van der Ende A, et al. Invasive pneumococcal disease: Clinical outcomes and patient characteristics 2-6 years after introduction of 7-valent pneumococcal conjugate vaccine compared to the pre-vaccine period, the Netherlands. Vaccine. 2016;34(8):1077-85.
- Gezondheidsraad - Vaccinatie van ouderen tegen pneumokokken (2023) 2023 [Available from: https://www.gezondheidsraad.nl/onderwerpen/vaccinaties/alle-adviezen-over-vaccinaties/vaccinatie-van-ouderen-tegen-pneumokokken-2023.
Infectieziekten Bulletin - maart 2024
- Nederlandse reizigers in het mondiale dorp: de opkomst en ondergang van reis-gerelateerde infectieziekten
- Infectieziektesurveillance bij de GGD vóór de covid-pandemie: een mixed-methods onderzoek, 2018-2019
- Evaluatie van surveillance systeem voor invasieve pneumokokkenziekte in volwassenen van 60 jaar en ouder, 2021-2022
- De opkomst van kunstmatige intelligentie in de publieke gezondheidszorg vraagt om medisch leiderschap
- Titercontrole bij kinderen van moeders met hepatitis B
- Over het Infectieziekten Bulletin