Infectieziekten Bulletin, februari 2026
Auteurs
Ines Figaroa1, Daan Vermeulen1, Ellen van Jaarsveld3, Roan Pijnacker2, Stijn Raven1,3
- (Gemeentelijke Gezondheidsdienst) regio Utrecht, afdeling Infectieziektebestrijding, Zeist, Nederland
- Rijksinstituut voor Volksgezondheid en Milieu, Centrum Infectieziektebestrijding, Bilthoven, Nederland
- Academische werkplaats AMPHI, afdeling Eerstelijnsgeneeskunde, (Radboud University Medical Centre), Nijmegen
Introductie
Bron- en contactonderzoek (BCO) is een essentieel instrument binnen de infectieziektebestrijding. Hierbij interviewen medewerkers van de gemeentelijke gezondheidsdiensten (GGD) geïnfecteerde personen om besmettingsbronnen te achterhalen en om recente contacten te identificeren en te informeren over het risico op besmetting en over preventieve maatregelen, zoals laten testen, in quarantaine gaan, of symptomen in de gaten houden (1). Hoewel deze methode goed werkt bij kleinere uitbraken, kan deze aanpak bij grootschalige uitbraken een uitdaging vormen. De grote hoeveelheid patiënten en (mogelijke) contacten die geïnformeerd moeten worden, maken het proces arbeidsintensief en tijdrovend (2,3). Dit kan leiden tot een langere doorlooptijd van het oppakken van een melding tot het informeren van een geïnfecteerde persoon en zijn/haar contacten – hetgeen het risico op secundaire infecties vergroot (4). Ook kan het mogelijk zorgen voor een vermindering van de kwaliteit en compleetheid van de verzamelde (Bron- en contactonderzoek)-data, omdat de focus komt te liggen op het zo snel mogelijk afhandelen van nieuwe meldingen. Om dit probleem te ondervangen hebben veel landen, waaronder Nederland, digitale hulpmiddelen ontwikkeld die het BCO potentieel sneller en efficiënter maken (5,6).
Tijdens de COVID-19-pandemie, veroorzaakt door het virus (severe acute respiratory syndrome)-CoV-2, had de (Gemeentelijke Gezondheidsdienst) regio Utrecht (GGDrU) vanaf 15 januari 2021 een systeem ingevoerd (Coronacare) dat een groot deel van het BCO digitaal liet verlopen. Na een positieve SARS-CoV-2-testuitslag werd bij een telefonisch gesprek nagegaan of het BCO digitaal kon plaatsvinden. Indien mogelijk kregen burgers automatisch een link naar een online BCO-vragenlijst toegestuurd per mail. Wanneer dit niet mogelijk was, bijvoorbeeld vanwege een taalbarrière of omdat de patiënt dat niet wilde, werd het BCO samen met een GGD-medewerker ingevuld. Ook bij geen respons op de online BCO-vragenlijst werd het BCO samen met een GGD-medewerker doorlopen. Dit systeem werd ingevoerd om de werklast bij hoge infectiedruk te verlichten en stelde burgers in staat om een groot deel van het BCO digitaal in te vullen voordat een telefonische follow-up plaatsvond.
De toegevoegde waarde van digitaal ondersteund BCO tijdens de pandemie is voor de praktijk nog niet goed in kaart gebracht (6,7). Dit is wel van belang om te doen, omdat het bijdraagt aan de discussie over de modernisering van het BCO en hoe digitale middelen kunnen helpen om snelheid en kwaliteit van het BCO te behouden. Een effectievere aanpak van toekomstige epidemieën en pandemieën kan hierdoor mogelijk worden ondersteund. Het doel van dit onderzoek is het onderzoeken van zowel de doorlooptijd van melding bij de GGD tot het informeren van de persoon met een positieve SARS-CoV-2-testuitslag, als de compleetheid van de BCO-data. Hiervoor zijn twee periodes met elkaar vergeleken: een periode waarin sprake was van digitaal ondersteund BCO en een vergelijkbare periode waarin sprake was van ‘traditioneel’ BCO zonder digitale ondersteuning.
Methode
Onderzoeksopzet
Dit observationele onderzoek maakt gebruik van routinematig verzamelde gegevens tijdens de COVID-19-pandemie. Met deze gegevens kan kwantitatief worden onderzocht in hoeverre een digitaal ondersteunde BCO-periode de doorlooptijd van binnenkomst van de melding bij de GGD tot het informeren van de patiënt beïnvloedt. Daarnaast kan worden bepaald of het leidt tot een meer complete aanlevering van informatie aan het RIVM, in vergelijking met een traditionele BCO-periode. Aanvankelijk was de doelstelling om ook de doorlooptijd van aanvang melding tot het informeren van contacten van de patiënt en de doorlooptijd van aanvang melding tot het informeren van het RIVM (de Osiris-melding) te vergelijken tussen een digitaal ondersteunde BCO-periode en een traditionele BCO-periode. Maar vanwege de gebrekkige betrouwbaarheid en datakwaliteit van deze variabelen was het beantwoorden van deze vraagstelling niet mogelijk.
Onderzoekspopulatie
De onderzoekspopulatie bestaat uit personen met een positieve SARS-CoV-2-testuitslag gemeld bij GGDrU binnen twee periodes:
- Van 11 november 2020 tot en met 9 december 2020 – zij kregen het traditionele BCO
- Van 22 februari 2021 tot en met 21 maart 2021 – zij kregen het digitaal ondersteunde BCO
Deze periodes zijn geselecteerd omdat zij vergelijkbaar waren wat betreft infectiedruk en capaciteit van personeel ten tijde van de COVID-19-pandemie. In dit geval was dat BCO fase 1: de meest uitgebreide vorm bij het informeren en monitoren van contacten rond de geïnfecteerde persoon. Ook had de bevolking in deze periodes een vrijwel gelijke houding ten opzichte van de coronamaatregelen, zoals onderzocht in het landelijke gedragsonderzoek(8).
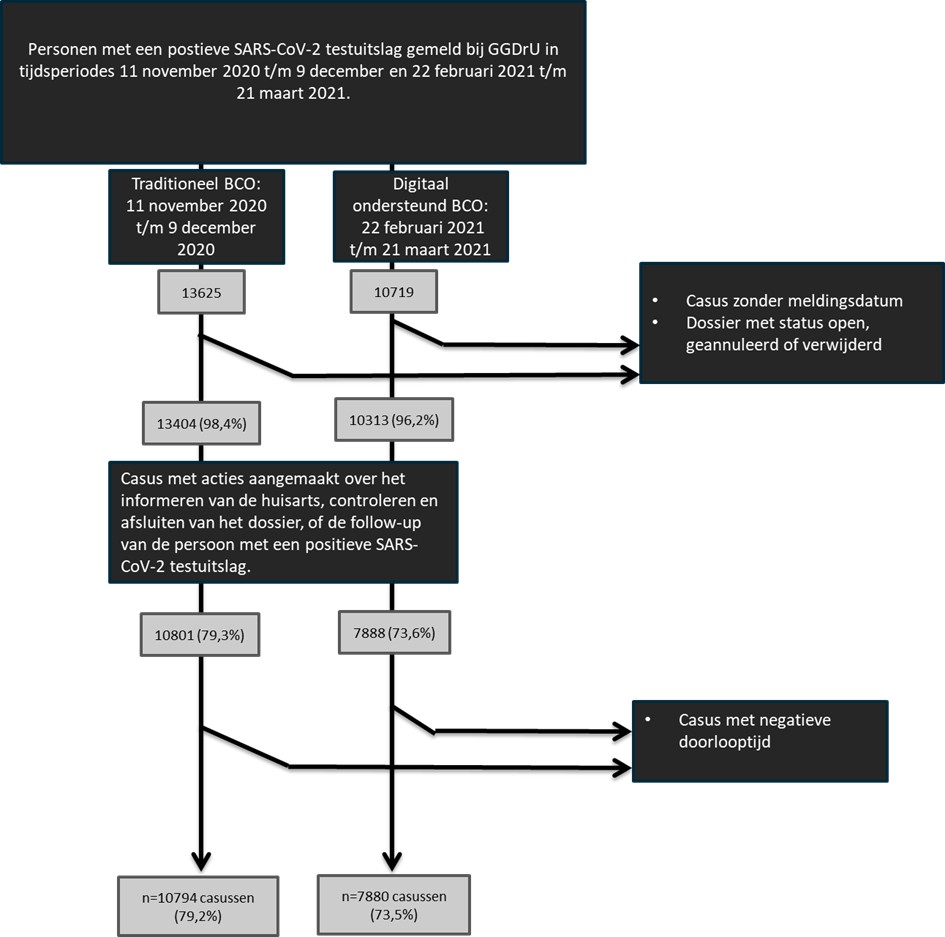
Personen met een positieve SARS-CoV-2-testuitslag zonder meldingsdatum zijn geëxcludeerd. Ook open, geannuleerde of verwijderde dossiers zijn uitgesloten van inclusie. Daarnaast zijn personen met een positieve SARS-CoV-2-testuitslag uitgesloten wanneer er was geregistreerd dat het BCO was afgerond vóórdat de persoon was gemeld bij de GGD. Uiteindelijk zijn er in deze studie n=10.794 personen geïncludeerd in de periode met traditioneel BCO en n= 7.880 personen in periode met digitaal ondersteund BCO, allen met een positieve SARS-CoV-2-testuitslag, zie Figuur 1.
Figuur 1 - Personen met een positieve SARS-CoV-2 testuitslag gemeld bij GGDrU in tijdsperiodes 11 november 2020 t/m 9 december en 22 februari 2021 t/m 21 maart 2021
Dataverzameling en variabelen
Voor dit onderzoek zijn gegevens geëxtraheerd en verzameld uit drie systemen: HpZone, (information system) en Coronacare. HpZone is gebruikt om patiëntkenmerken en datumvariabelen te verzamelen, zoals geslacht, leeftijd, melddatum geïnfecteerde persoon op indicatie van een positieve test, en informatie over personen die eerder als contact zijn geregistreerd. Dit verwijst naar personen die aanvankelijk als contact van een persoon met een positieve SARS-CoV-2-testuitslag in HpZone zijn geregistreerd en later zelf als SARS-CoV-2-geïnfecteerd zijn gemeld. OSIRIS is gebruikt voor de verzameling van gegevens die aan het RIVM zijn aangeleverd, zoals datum eerste ziektedag, ziekenhuisopname, reisgeschiedenis en de setting van besmetting (bijvoorbeeld werkplek, basisonderwijs of langdurige zorg). Coronacare diende om personen met een positieve SARS-CoV-2-testuitslag te identificeren die gebruik maakten van digitaal ondersteund BCO.
Om de doorlooptijd te bepalen zijn datumvariabelen gebruikt. Dit betrof de datum van melding van de geïnfecteerde persoon bij de GGD en acties als het informeren van de huisarts, het controleren en afsluiten van dossiers en de follow-up van een geïnfecteerde persoon. De doorlooptijd in deze studie wordt gedefinieerd als het aantal dagen tussen de datum van de melding bij GGDrU en de datum van de eerst gelogde actie, waarbij het gaat om één van de volgende acties: het informeren van de huisarts, het controleren en afsluiten, of de follow-up van de geïnfecteerde persoon. Deze acties hielden namelijk in dat een GGDrU-medewerker de geïnfecteerde persoon had gesproken en geïnformeerd.
Om de compleetheid van BCO-data te bepalen is in OSIRIS gekeken naar ingevulde, ontbrekende en onbekende gegevens. Compleetheid wordt gedefinieerd als het percentage van ingevulde gegevens ten opzichte van het totaal geregistreerde gegevens.
Data-analyse
Descriptieve analyses zijn uitgevoerd van de kenmerken van personen met COVID-19, uitgesplitst naar de periodes van traditioneel BCO en digitaal ondersteund BCO. Verschillen tussen groepen voor categorische data zijn geanalyseerd met een Chi-square-test of Fisher’s exact-test en voor continue data met een Mann-Whitney U-test. Een logistische regressie van risicofactoren voor de doorlooptijd is uitgevoerd. Hierbij is de doorlooptijd dichotoom gecategoriseerd als minder dan één dag, of één dag of langer. Deze indeling naar doorlooptijd is gebaseerd op de studie van Kretschmar et al., die doorlooptijden van het testen en het informeren van een persoon met COVID-19 hebben gemodelleerd op het effect op doorgaande COVID-19-transmissie (9). Om nog een reductie op doorgaande COVID-19-transmissie te hebben zou de doorlooptijd tussen melding aan de GGD en het informeren van de patiënt binnen één dag moeten liggen (bij een mediane doorlooptijd van twee dagen voor de periode tussen het ontstaan van klachten en het verkrijgen van een testuitslag) (10).
Odds ratio’s zijn berekend in een univariabel en multivariabel model. Variabelen met een p-waarde < 0,10 in het univariabele model, zijn meegenomen in het multivariabele model. Modererende effecten van geslacht, leeftijd, ziekenhuisopname en personen met een positieve SARS-CoV-2-testuitslag die eerder als contact waren geregistreerd op de doorlooptijd zijn onderzocht met een stratificatieanalyse. Verschillen tussen tijdsperiodes in de compleetheid van gegevens zijn getoetst met een Z-test. In deze studie is een significantie-level (α) van 0,05 gehanteerd, tenzij anders aangegeven. Alle analyses zijn uitgevoerd in R.
Resultaten
Karakteristieken van de studiepopulatie
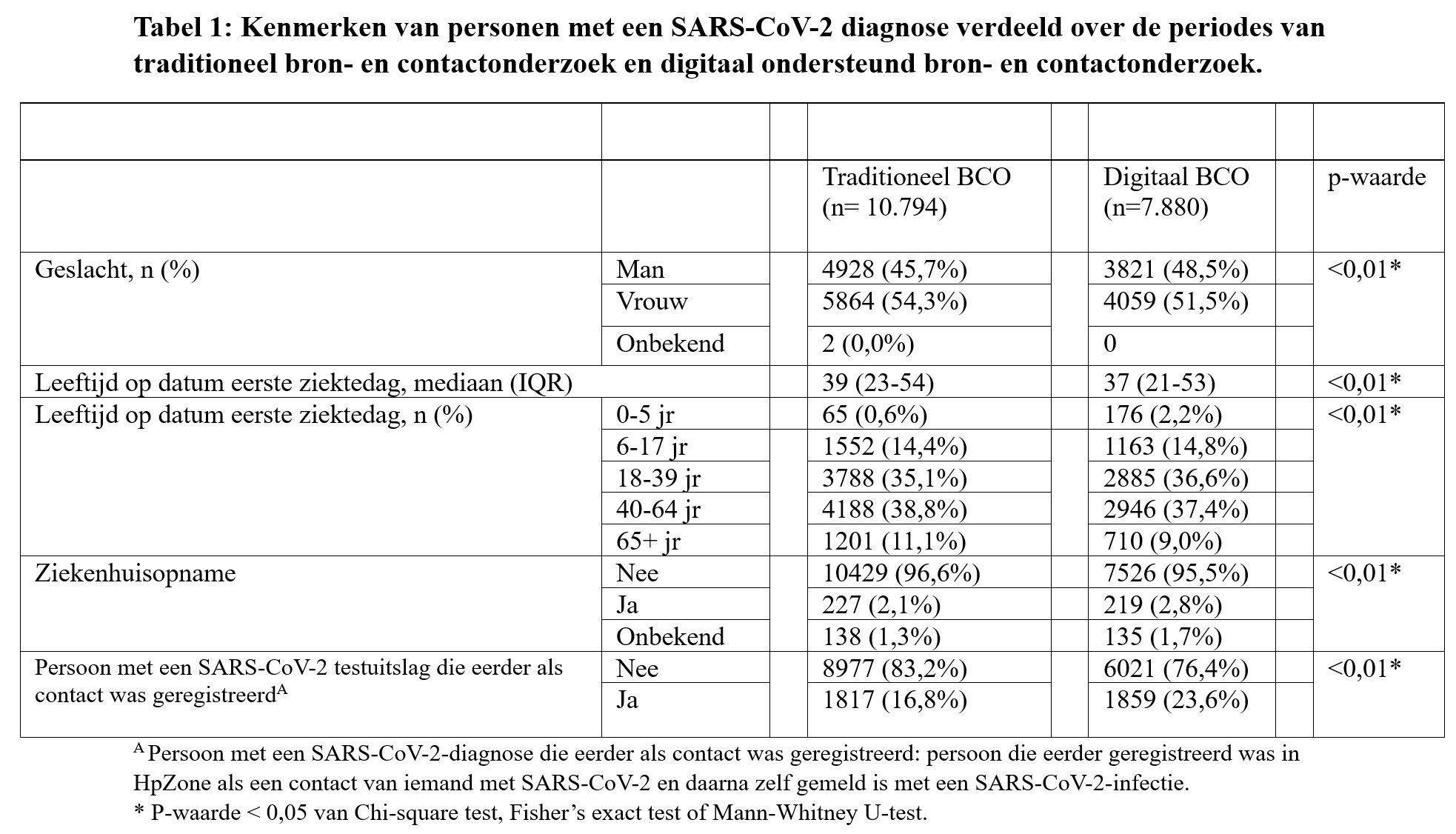
Tussen de periode met traditioneel BCO en de periode met digitaal ondersteund BCO zijn significante verschillen gevonden in alle onderzochte variabelen: geslacht, leeftijd, ziekenhuisopname en het percentage persoon met een positieve SARS-CoV-2-testuitslag die eerder als contact was geregistreerd. De resultaten in Tabel 1 tonen aan dat in zowel de periode met traditioneel BCO, als de periode met digitaal ondersteund BCO, personen met een SARS-CoV-2-testuitslag vaker vrouw waren (traditioneel BCO: 52%; digitaal BCO: 54%). De mediane leeftijd was 39 jaar (IQR: 23-54) in de populatie met digitaal ondersteund BCO en 37 jaar (IQR: 21-53) in de populatie met traditioneel BCO. In de periode met digitaal ondersteund BCO was het aandeel personen met een SARS-CoV-2-diagnose die eerder als contact van een persoon met SARS-CoV-2 waren geregistreerd 24%. Dat is hoger dan het aandeel van 17% in de periode met traditioneel BCO.
Doorlooptijd van melding bij de (Gemeentelijke Gezondheidsdienst) tot het informeren van de geïnfecteerde persoon
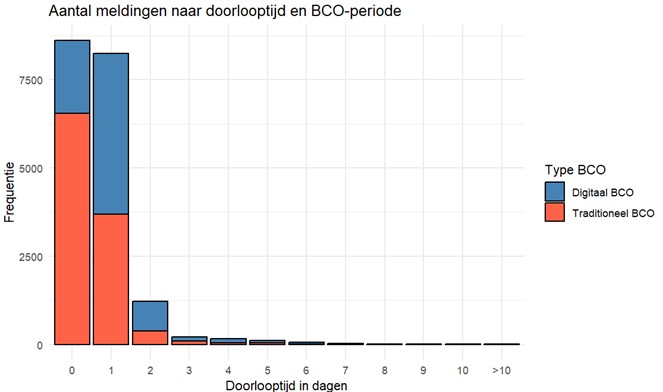
De mediane doorlooptijd van melddatum bij de GGD tot het informeren van de persoon met een positieve (severe acute respiratory syndrome)-CoV-2-diagnose is 0 dagen (min-max: 0-32) in de periode van traditioneel (Bron- en contactonderzoek), vergeleken met een mediaan van 1 dag (min-max: 0-29) in de periode van digitaal BCO. Dit verschil is significant (p < 0,01). Het merendeel (61%) van de personen met een positieve SARS-CoV-2-testuitslag in periode van traditioneel BCO heeft een doorlooptijd van minder dan 1 dag. In de periode van digitaal BCO heeft het merendeel (74%) een doorlooptijd van één dag of langer. Zie Figuur 2 voor een overzicht van de verdeling in een histogram.
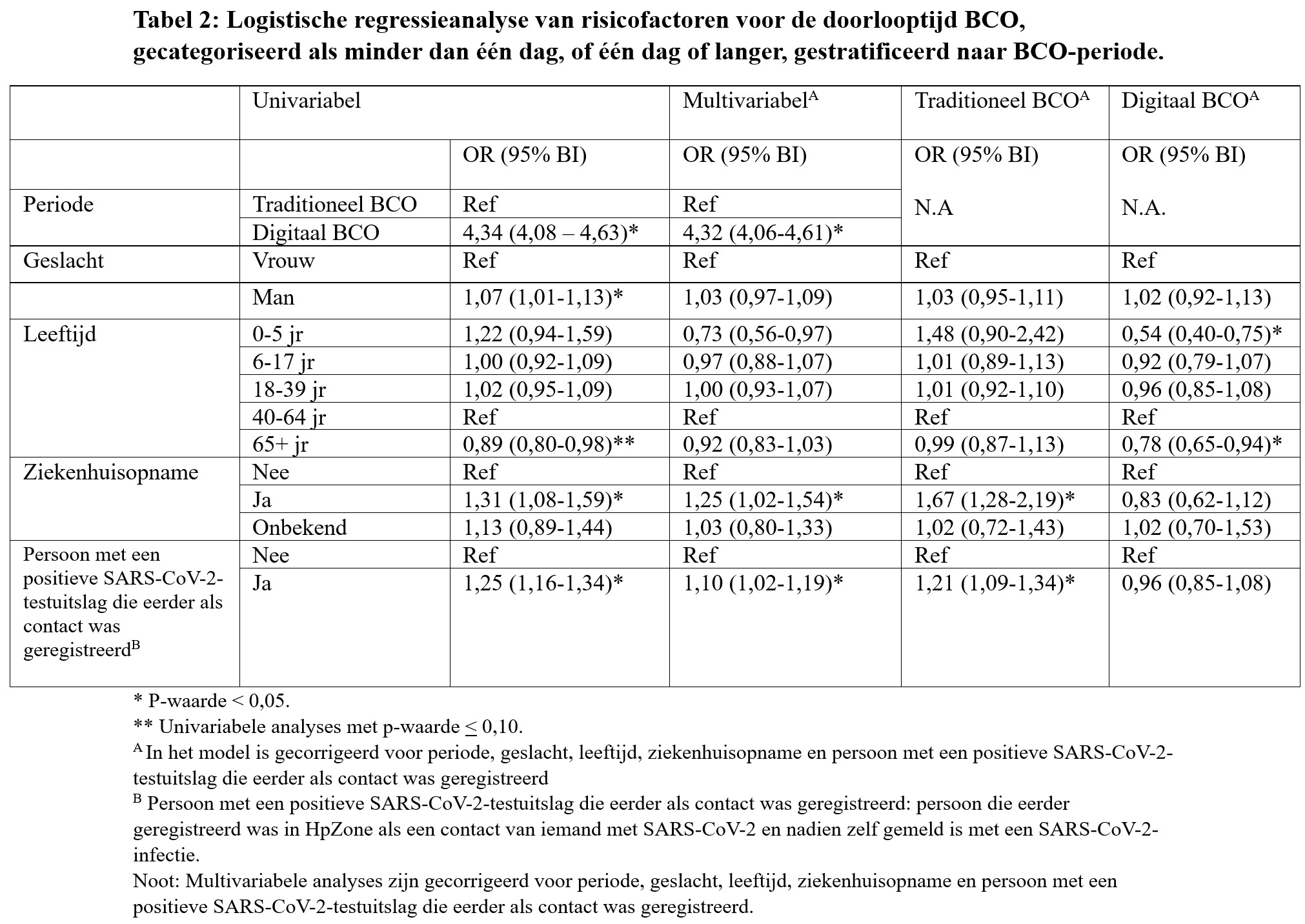
De univariabele en multivariabele analyses worden in Tabel 2 getoond. In het univariabele model was de doorlooptijd significant langer in de periode met digitaal BCO dan in de periode met traditioneel BCO. De doorlooptijd was ook significant langer voor mannen, voor personen met een SARS-CoV-2-testuitslag opgenomen in het ziekenhuis en voor personen met een SARS-CoV-2 testuitslag die eerder als contact stonden geregistreerd. Voor de 65-plussers was de doorlooptijd marginaal significant korter (p-waarde < 0,10). Na correctie in het multivariabele model, was de doorlooptijd nog steeds significant langer in de periode met digitaal BCO ten opzichte van traditioneel BCO (OR: 4,32; 95% BI: 4,06-4,61). Ook was de doorlooptijd significant langer bij personen met een SARS-CoV-2-testuitslag met een ziekenhuisopname (OR: 1,25; 95% BI: 1,02-1,54) en personen met een SARS-CoV-2-testuitslag die eerder als contact waren geregistreerd (OR: 1,10; 95% BI: 1,02-1,19). De variabelen geslacht en leeftijd waren na correctie niet significant.
De analyses waren ook gestratificeerd naar BCO-periode, zie Tabel 2. Na stratificatie is het effect van leeftijd op kortere doorlooptijden in de digitale BCO-periode sterker geworden. In de groep 0-5-jarigen daalde de OR van 0,73 (95% BI: 0,56–0,97) naar 0,54 (95% BI: 0,40–0,75), en bij 65-plussers van 0,92 (95% BI: 0,83–1,03) naar 0,78 (95% BI: 0,65–0,94). Beide effecten werden na stratificatie significant. In de traditionele BCO-periode is het effect van leeftijd op langere doorlooptijden groter geworden. De OR nam bij 0-5-jarigen toe naar 1,48 (95% BI: 0,90–2,42), maar het effect was niet significant. Na stratificatie was het effect van ziekenhuisopname op langere doorlooptijden sterker geworden in de traditionele BCO-periode. De OR nam bij een ziekenhuisopname toe van 1,25 (95% BI: 1,02-1,54) naar 1,67 (95% BI: 1,28-2,19). Bij digitaal BCO was dit effect niet significant. Het effect van een langere doorlooptijd bij personen met een positieve SARS-CoV-2-testuitslag die eerder als contact waren geregistreerd is sterker geworden in de periode met traditioneel BCO. De OR nam toe van 1,10 (95% BI: 1,02-1,19) naar 1,21 (95% BI: 1,09-1,34). In de periode met digitaal BCO daalde de OR naar 0,96 (95%: 0,85-1,08), maar het effect was niet significant. Er zijn geen verschillen gevonden in het effect van geslacht op de doorlooptijd tussen de BCO-periodes.
Figuur 2. Doorlooptijd van de melding bij de GGD tot het informeren van de persoon met een positieve SARS-CoV-2-testuitslag, verdeeld over de periodes van digitaal ondersteund BCO en traditioneel BCO. De mediane doorlooptijd was 0 dagen bij traditioneel BCO en 1 dag bij digitaal BCO (p < 0,01).
Compleetheid BCO-data
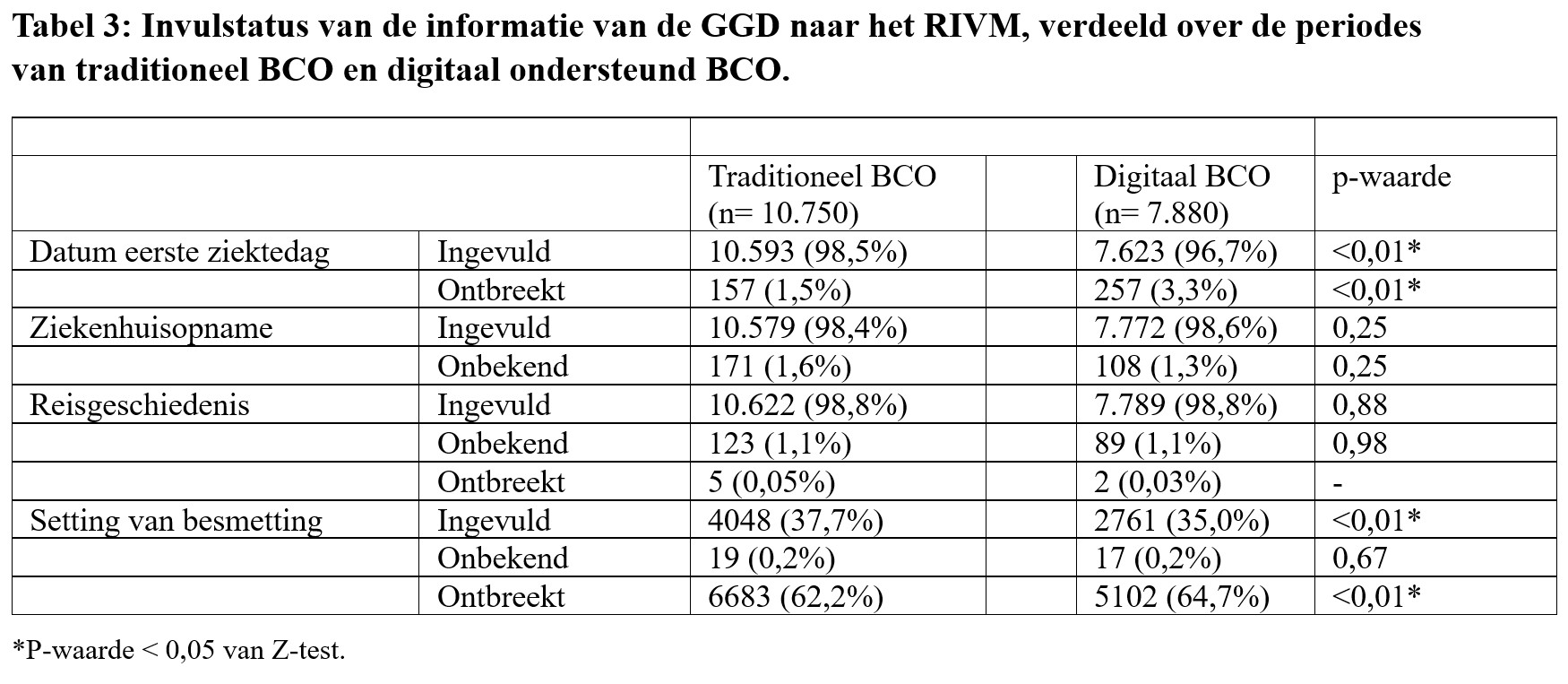
De invulstatus van de (Bron- en contactonderzoek)-data, verdeeld over de twee periodes, staat in Tabel 3. BCO-data was grotendeels ingevuld, met uitzondering van informatie over de setting van besmetting. Voor deze variabele ontbrak het merendeel van de gegevens, zowel in de periode van traditioneel BCO (62%) als in de periode van digitaal BCO (65%). Er waren significante verschillen in invulstatus “ingevuld” en “ontbreekt” tussen de BCO-periodes voor de variabele ‘setting van besmetting’.
De variabele ‘datum eerste ziektedag’ was in periode traditioneel BCO 99% ingevuld in vergelijking met 97% in periode digitaal BCO. Voor de variabele ‘datum eerste ziektedag’ was een significant verschil gevonden tussen BCO-periodes in invulstatus “ingevuld” en “ontbreekt”. De variabele ‘ziekenhuisopname’ was in periode traditioneel BCO 98,4% ingevuld, in vergelijking met 98,6% in periode digitaal BCO. De variabele ‘reisgeschiedenis’ was in zowel periode traditioneel BCO en digitaal BCO 99% ingevuld.
Discussie en conclusie
Korte samenvatting
Tijdens de periode met digitaal (Bron- en contactonderzoek) was de doorlooptijd langer dan tijdens de periode met traditioneel BCO. Dit betekent dat er bij digitaal BCO meer tijd zat tussen het moment van de melding bij de (Gemeentelijke Gezondheidsdienst) en het informeren van de persoon met een positieve testuitslag. Daarnaast blijkt leeftijd, specifiek bij 0-5-jarigen en 65-plussers, in de periode van digitaal BCO geassocieerd te zijn met kortere doorlooptijden. In de periode van traditioneel BCO blijkt een ziekenhuisopname en eerdere registratie als contact van een persoon met (severe acute respiratory syndrome)-CoV-2 geassocieerd te zijn met langere doorlooptijden.
In compleetheid van de data is er geen duidelijk verschil tussen de twee periodes. Gegevens uit het BCO met betrekking tot datum eerste ziektedag, ziekenhuisopname en reisgeschiedenis waren in beide periodes over het algemeen ingevuld en compleet. Informatie over de setting van besmetting werd in zowel de traditionele als de digitale BCO-periode beperkt ingevuld. Dit laat ruimte voor verbetering in de volledigheid van de registratie.
Vanwege beperkingen in de validiteit van de geregistreerde gegevens moeten de conclusies met voorzichtigheid worden geïnterpreteerd. Een herziening op de inrichting van het registratiesysteem is nodig om toekomstige BCO-processen te optimaliseren en te duiden.
Literatuur
In de literatuur worden verschillende voordelen genoemd voor het gebruik van digitaal ondersteund BCO, waaronder:
- het versnellen van processen
- het verbeteren van de efficiëntie
- het vergroten van het bereik bij opsporen van contacten
Deze studie laat echter zien dat digitaal ondersteund BCO niet per definitie leidt tot kortere doorlooptijden. Dit komt overeen met literatuur die heeft aangetoond dat digitaal ondersteunde contactopsporing vergelijkbare of zelfs langere doorlooptijden kent dan traditionele contactopsporing (11–13). Het is belangrijk om daarbij aan te geven dat deze studies verschillende definities van doorlooptijd hebben gehanteerd.
De vertragingen in doorlooptijden lijken voornamelijk te worden veroorzaakt door casusregistratie en gegevensverwerking, en niet door de daadwerkelijke uitvoering van de contactopsporing. Onderzoekers benoemen dat technologische en logistieke beperkingen (zoals netwerkwerkdekking en serververwerking), lage deelname aan de studie en ontbreken van menselijke opvolging de werking van digitaal contactopsporing vertraagden. Bij traditioneel contactopsporing speelden deze administratieve tussenstappen en technische afhankelijkheden een kleinere rol. Dit benadrukt dat tijdswinst in één stap van het proces niet automatisch leidt tot een kortere totale doorlooptijd. Mogelijk hebben deze administratieve tussenstappen of technische afhankelijkheden ook bij het digitaal ondersteund BCO een rol gespeeld in de langere doorlooptijd. Er zat tijd tussen het versturen van de digitale vragenlijst en het contact opnemen met de persoon om de vragenlijst door te nemen over het BCO. In het klassiek BCO was deze vertraging in tijd mogelijk niet aanwezig en werd direct contact opgenomen om het BCO af te nemen.
Uit eerder onderzoek blijkt dat burgers over het algemeen een positieve houding hebben tegenover zelfstandig uitgevoerd contactonderzoek (7). Dit sluit aan bij onze bevindingen, waaruit blijkt dat digitaal verstuurde BCO-vragenlijsten grotendeels volledig werden ingevuld. In 7% van de gevallen werd de vragenlijst niet digitaal ingevuld. In deze situaties vulde een GGD-medewerker de vragenlijst samen met de betrokkene in. Dit waren met name patiënten in de leeftijdsgroep 0-5, 40-64 en 65-plussers.
Beperkingen
Deze studie kent enkele beperkingen. Omdat twee verschillende periodes worden vergeleken, moet rekening worden gehouden met mogelijke selectiebias. Hoewel bij de vergelijking van de twee periodes is gestreefd naar vergelijkbare omstandigheden (gelijk aantal COVID-19-meldingen per week, inschaling van BCO en houding tegenover coronamaatregelen – zoals gemeten via het landelijk gedragsonderzoek), blijft het lastig om volledig gelijkwaardige periodes te kiezen. Vanwege de contextuele verschillen tussen de periodes, moeten de resultaten met voorzichtigheid geïnterpreteerd worden. Zo waren in beide periodes de gedragsregels op het gebied van testen niet opgenomen, was in de periode met traditioneel BCO de vaccinatiecampagne nog niet gestart en waren de overheidsmaatregelen in de periode met digitaal BCO strenger. De Stringency Index, een maat voor hoe streng overheidsmaatregelen zijn, waarbij een hogere score duidt op strengere overheidsmaatregelen, bedroeg in de periode met traditioneel BCO 62 en steeg in de periode met digitaal ondersteund BCO naar 79 en 75 (14).
Aangezien beide BCO-periodes ruim drie maanden na elkaar lagen, is een verandering van werkwijze in de registratie van BCO op de door ons gebruikte velden voor de doorlooptijd niet waarschijnlijk, maar ook niet in het geheel uit te sluiten. Een andere mogelijke beperking in deze studie is het meten van de doorlooptijd in dagen in plaats van in uren. Mogelijk is deze werkwijze niet sensitief genoeg en geeft een doorlooptijd in uren beter inzicht in eventuele verschillen tussen digitaal en traditioneel BCO.
Een sterk punt van deze studie is dat voor het eerst de doorlooptijd in kaart is gebracht van de COVID-19-melding aan de GGD tot aan het informeren van de geïnfecteerde persoon. Een eerdere studie in Nederland naar doorlooptijden van testen voor COVID-19 en het BCO bij de GGD publiceerde geen gegevens over doorlooptijden na melding van de COVID-19-uitslag aan de GGD vanwege een variabele datakwaliteit en het hanteren van verschillende definities binnen GGD’en over deze tijdsperiode (10). Die studie liet ook zien dat in veel gevallen de doorlooptijd van testen en het BCO niet snel genoeg was om veel impact te hebben op doorgaande COVID-19-transmissie. Ook in onze studie lag het aandeel personen dat binnen één dag geïnformeerd werd van een positieve testuitslag tussen de 26% (digitale periode) en 61% (traditionele periode).
Een ander sterk punt van deze studie is de omvang van de dataset. Echter, niet alle relevante variabelen konden worden meegenomen. Dit beperkt de interpretatie van de resultaten. De analyse richt zich uitsluitend op de doorlooptijd tussen de melding bij de GGD en het informeren van de geïnfecteerde persoon, terwijl het oorspronkelijke plan was om ook de doorlooptijd tot het informeren van contacten en het RIVM te analyseren.
Implicaties
Er was tot nu toe beperkt onderzoek gedaan naar de toegevoegde waarde van digitaal BCO. Dit onderzoek vormt een eerste poging om de toegevoegde waarde van digitaal ondersteund BCO te analyseren op basis van data van GGD-professionals. Het evalueren van het BCO-proces met routinematig verzamelde data bleek niet eenvoudig. In deze studie is vastgesteld dat bepaalde gegevens voor het monitoren van de doorlooptijden van het BCO-proces niet gestandaardiseerd waren in het systeem en daardoor moeilijk toegankelijk of onvolledig waren. Voor toekomstig onderzoek naar digitaal BCO is het essentieel om de registratie te versterken. Dit houdt in dat niet alleen inhoudelijke gegevens worden vastgelegd, maar ook het registreren van processtappen. Een duidelijke vastlegging van start- en eindvelden binnen het BCO-proces en de systematische registratie van processtappen, zoals het informeren van geïnfecteerde personen en contacten met een tijdstempel, zijn hierbij cruciaal. Daarvoor zijn exacte tijdstippen nodig van alle relevante procesmomenten in het BCO, zoals hierboven benoemd.
Daarnaast is het wenselijk dat alle contacten gekoppeld aan personen met een positieve testuitslag volledig kunnen worden vastgelegd en kunnen worden geëxporteerd voor onderzoek. De uitvoering hiervan vereist aanvullend op een technische verbeterslag van de data-infrastructuur, aandacht voor pseudonimisatie, heldere afspraken over datadeling en een veilige data-infrastructuur. Door deze verbeteringen kan de effectiviteit van digitaal ondersteund BCO niet alleen beter worden geëvalueerd, maar wordt ook de kwaliteit van de verzamelde gegevens verhoogd. Deze inzichten zijn relevant voor toekomstig onderzoek en de herziening van het informatievoorzieningenlandschap, waarin een nieuw registratiesysteem wordt ontwikkeld voor de infectieziektebestrijding.
Conclusie
Resultaten van deze studie geven aanwijzingen dat digitaal ondersteund BCO leidt tot langere doorlooptijden en geen verbetering oplevert in datacompleetheid ten opzichte van traditioneel BCO. Meer onderzoek is nodig om dit te bevestigen of ontkrachten. Om betere uitspraken te kunnen doen over de effectiviteit en meerwaarde van digitaal BCO is betere en gestandaardiseerde dataverzameling noodzakelijk. Door in de toekomst aandacht te besteden aan gestructureerde en gestandaardiseerde vastlegging van processtappen, kan niet alleen de evaluatie van BCO verbeteren, maar ook de inzetbaarheid van digitaal BCO binnen infectieziektebestrijding worden geoptimaliseerd.
- Chowdhury MJM, Ferdous (Multiple Sclerose), Biswas K, Chowdhury N, Muthukkumarasamy V. COVID-19 Contact Tracing: Challenges and Future Directions. IEEE Access. 2020;8:225703-29.
- Duthie S, Black C, Douglas G, Jackson AD, Webster D. Tuberculosis outbreak associated with a mosque: challenges of large scale contact tracing. Eurosurveillance [Internet]. 18 december 2008 [geciteerd 7 augustus 2025];13(51).
- Grammens T, Schirvel C, Leenen S, Shodu N, Hutse V, Mendes da Costa E, e.a. Ongoing measles outbreak in Wallonia, Belgium, December 2016 to March 2017: characteristics and challenges. Eurosurveillance. 27 april 2017;22(17):30524.
- Gardner BJ, Kilpatrick AM. Contact tracing efficiency, transmission heterogeneity, and accelerating COVID-19 epidemics. PLOS Comput Biol. 17 juni 2021;17(6):e1009122.
- Braithwaite I, Callender T, Bullock M, Aldridge RW. Automated and partly automated contact tracing: a systematic review to inform the control of COVID-19. Lancet Digit Health. november 2020;2(11):e607-21.
- Helms YB, Hamdiui N, Eilers R, Hoebe C, Dukers-Muijrers N, van den Kerkhof H, e.a. Online respondent-driven detection for enhanced contact tracing of close-contact infectious diseases: benefits and barriers for public health practice. BMC Infect Dis. 16 april 2021;21(1):358.
- Helms YB, van der Meer A, Crutzen R, Ferreira JA, Kretzschmar MEE, Timen A, e.a. Determinants of Citizens’ Intention to Participate in Self-Led Contact Tracing: Cross-Sectional Online Questionnaire Study. JMIR Public Health Surveill. 30 oktober 2024;10:e56943.
- Resultaten onderzoek gedragsregels en welbevinden | RIVM [Internet]. [geciteerd 28 januari 2026].
- Kretzschmar ME, Rozhnova G, Bootsma MCJ, Boven M van, Wijgert JHHM van de, Bonten MJM. Impact of delays on effectiveness of contact tracing strategies for COVID-19: a modelling study. Lancet Public Health. 1 augustus 2020;5(8):e452-9.
- Bosdriesz JR, den Boogert EM, van Dijken S, Dukers-Muijrers NHTM, Götz HM, Goverse IE, e.a. The influence of case factors and system factors on the timeliness of testing and contact tracing for COVID-19 in The Netherlands. Eur J Public Health. 8 juli 2025;ckaf109.
- Ter Haar W, Bosdriesz J, Venekamp (Responsible Person), Schuit E, van den Hof S, Ebbers W, e.a. The epidemiological impact of digital and manual contact tracing on the SARS-CoV-2 epidemic in the Netherlands: Empirical evidence. PLOS Digit Health. december 2023;2(12):e0000396.
- Danquah LO, Hasham N, MacFarlane M, Conteh FE, Momoh F, Tedesco AA, e.a. Use of a mobile application for Ebola contact tracing and monitoring in northern Sierra Leone: a proof-of-concept study. BMC Infect Dis. 18 september 2019;19(1):810.
- Al-Kuwari MG, Nuaimi AAA, Semaan S, Gibb (Joint meeting), AbdulMajeed J, Romaihi HEA. Effectiveness of Ehteraz digital contact tracing app versus conventional contact tracing in managing the outbreak of COVID-19 in the State of Qatar. BMJ Innov [Internet]. 1 oktober 2022 [geciteerd 7 augustus 2025];8(4).
- Max Roser (2021) - “What is the COVID-19 Stringency Index?” Published online at OurWorldinData.org.
Infectieziekten Bulletin - februari 2026
- Van centrumvorming naar verdere professionalisering en een pandemie
- Wonderlijke vraag: Een peuter die een slak opeet, is dat gevaarlijk
- Digitaal ondersteund bron- en contactonderzoek tijdens de COVID-19-pandemie: wat is de toegevoegde waarde?
- Ontwikkeling en evaluatie van e-learning voor huisartsen over infectieziekten bij kinderen
- Herzien en aangepast - Impact van de richtlijnwijziging voor chronische hepatitis B op GGD Hollands Midden